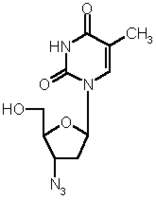
Azidothymidin / Zidovudin
Unveränderter Text aus ZCT Heft 4, 1987
Ergänzungen am Ende des Textes
Der amerikanische Wissenschaftler Horwitz synthetisierte in den 60er Jahren das Azidothymidin / Zidovudin (RETROVIR), das sich von der Nukleinsäurebase Thymidin ableitet. Es gehört zur Substanzklasse
der Nukleosid-Analoga (vgl. "ZCT" 7: 45, 1986).
Pharmakodynamik
Nukleoside sind in der Lage, als modifizierte Genombausteine an verschiedenen Punkten die Transkription (genetischer Informationsfluß von DNA zu mRNA) oder Translation (mRNA als Matrix für die
Synthese viraler Proteine) zu stören. Azidothymidin wird intrazellulär durch ein Enzym (Thymidinkinase) zum Triphosphat umgewandelt und steht dann alternativ zum physiologischen Nukleotid für den
Einbau in die DNA zur Verfügung. Dabei ist ein wesentlicher Schritt in der Replikation des HIV (Erreger des AIDS) die Transkription der viralen RNS in die virale DNA, ein Prozeß, der über die virale
"reverse Transkriptase" vermittelt wird. Er ist Thymidin-abhängig und wird von Zidovudin-Triphosphat gehemmt. Die Wirkung gegen HIV-reverse Transkriptase ist relativ selektiv mit einem Faktor 100 : 1
im Vergleich zu zellulären DNA-Polymerasen.
Die Wirkungsweise von Azidothymidin besteht also in der Hemmung der reversen Transkriptase. Die Wirkung der Substanz ist daher abhängig von der aktiven Replikation des HIV in der Wirtszelle. Das
bedeutet, daß das Latenzstadium, in dem das Pro-Virus ohne Replikation in die Wirts-DNA integriert ist, nicht beeinflußt wird. Gleichzeitig kann zwar die Virusvermehrung gehemmt werden, das Virus
selbst wird jedoch nicht abgebaut.
Mikrobiologie
Azidothymidin ist als Inhibitor der reversen Transkriptase gegen eine Vielzahl tierischer Retroviren wirksam. In vitro-Untersuchungen zeigten eine Inhibition von HIV I, HIV II, HTLV-Spezies, dem
Katzen-Leukämie-Virus und partiell auch des Epstein-Barr-Virus. Wirksame Konzentrationen zur teilweisen bis vollständigen Hemmung des HIV in H9-Zellen schwankten zwischen 0,01 mM bis 5,0 mM.
Gegen Viren ohne das Enzym "reverse Transkriptase" scheint Azidothymidin nicht aktiv zu sein.
Pharmakokinetik
Zidovudin kann sowohl parenteral als auch per os verabreicht werden. Allerdings ist die Substanz in der Bundesrepublik Deutschland nur in der oralen Form als Kapsel erhältlich. Nach Verabreichung von
2 mg/kg Körpergewicht werden nach ca. 1 Stunde Serumspitzenwerte von 1,5 bis 2 mmol/l erreicht. Mit Erhöhung der Dosis auf 5 mg/kg steigt proportional die Spitzenkonzentration auf ca. 5 mmol/l an.
Von besonderer Bedeutung ist die gute Penetration in das Interstitium, insbesondere in den Cerebrospinalraum. Vier Stunden nach Einnahme können Liquor-Konzentrationen bis zu 55 % der
korrespondierenden Serumspiegel gemessen werden. Die Serum-Eliminationshalbwertzeit beträgt 60 Minuten. Nur 14 % der applizierten Substanz finden sich im Urin. Das Chemotherapeutikum wird überwiegend
hepatisch durch Glukuronidierung (74 %) eliminiert. Nach intravenöser Verabreichung von 2,5 mg/kg über eine Stunde werden identische Serumspitzenspiegel gemessen wie nach der oralen Verabreichung von
5 mg/kg. Die Bioverfügbarkeit der Substanz, gemessen als das Verhältnis der Fläche unter der Kurve nach oraler und intravenöser Applikation, liegt bei 60 %.
Da das Nukleosid-Analogon kaum renal ausgeschieden wird, ist eine Dosisanpassung bei Niereninsuffizienz nicht notwendig. Aufgrund der hepatischen Metabolisierung müssen allerdings mögliche
Interaktionen mit Substanzen beachtet werden, die die Arzneimittel-abbauenden Enzyme der Leber beeinflussen. Hierzu gehören Paracetamol (BEN-U-RON) und Acetylsalicylsäure (ASPIRIN).
Interaktionen sind ferner möglich mit Substanzen, die nephrotoxische und myelotoxische Wirkungen entfalten können. Dazu gehören unter anderem: Cotrimoxazol (BACTRIM, EUSAPRIM), Diaminodiphenylsulphon
(DAPSON); Pyrimethamin (DARAPRIM), Fluorzytosin (ANCOTIL) sowie einige weitere Virustatika und Zytostatika. Probenecid (BENEMID) kann die Ausscheidung und den Abbau von Zidovudin verzögern.
Klinische Studien
Einer kleinen, jedoch nach virologischen, klinischen und immunologischen Gesichtspunkten vielversprechenden Phase-I-Studie folgte von Februar bis Juni 1986 in den USA eine doppelblind-randomisierte
Multicenter-Studie an 282 Patienten in einer Dosierung von 6-mal 250 mg Zidovudin per os. 160 der Patienten litten am Vollbild des AIDS mit Zustand nach Pneumocystis carinii-Pneumonie. Die restlichen
122 Patienten hatten ARC. Die Patienten gehörten alle der homosexuellen Risikogruppe an, drogenabhängige Patienten mit Kaposi-Sarkom oder mit Alkohol-Krankheit waren ausgeschlossen. Nach 6 Monaten
wurde eine Zwischenauswertung hinsichtlich der Letalität und Häufigkeit von schweren Komplikationen wie opportunistische Infektionen vorgenommen.
Die Ergebnisse dieser Analyse können wie folgt zusammengefaßt werden:
1. Die Häufigkeit von opportunistischen Infektionen wurde durch Zidovudin deutlich gesenkt.
2. Ein signifikanter Unterschied zeigte sich in der Letalität: während ein Patient unter Zidovudin-Therapie verstarb, kamen 16 Patienten der Placebogruppe innerhalb der ersten sechs Monate ad exitum.
3. Unter der Zidovudin-Behandlung stiegen die T-Helferzellen an, um dann wieder auf den Ausgangswert zurückzugehen. 4. In der Placebo-Gruppe fielen die T-Helferzellen deutlich unter den Ausgangswert ab.
5. p24-Antigenspiegel fielen unter Zidovudin deutlicher ab als unter Placebo. p24 ist ein Marker für die Progression der Erkrankung. Als Nebenwirkungen wurden besonders Anämien, Leukopenien, Nausea, Myalgien und Kopfschmerzen registriert.
Indikation
Vom Bundesgesundheitsamt wurden bisher nur schwere Manifestationen von Infektionen durch das humane Immundefizienz-Virus (HIV) bei Patienten mit erworbenem Immunmangel-Syndrom oder
AIDS-related-Komplex als Anwendungsgebiete für das neue Medikament definiert. Die empfohlene Dosis beträgt 6-mal 200 bis 300 mg oral. Bei Hämoglobinwerten zwischen 7,5 und 9 g/dl oder Mangel an
neutrophilen Granulozyten (zwischen 750 und 1000 / ml) wird eine Dosisanpassung auf 3-mal 200 bis 300 mg Azidothymidin pro Tag erfolgen. Die Dauer der Behandlung muß individuell festgelegt
werden.
Nebenwirkungen
Die Nebenwirkungen betreffen vorwiegend das Knochenmark. Am empfindlichsten reagieren Erythropoese und Leukopoese, während die Thrombozyten relativ unempfindlich sind. So werden meistens nach sechs
Wochen Behandlung Anämien und Neutropenien beobachtet. Als weitere Nebenwirkungen wurden Übelkeit, Kopfschmerzen, Hautausschlag, Bauchschmerzen, Fieber, Myalgien, Parästhesien, Erbrechen,
Schlaflosigkeit und Appetitlosigkeit beschrieben. Störungen, bei denen der Zusammenhang zu der Medikation unklar blieb, waren allgemeine Schwäche, Krankheitsgefühl, Schläfrigkeit, Durchfall,
Schwindel, Schweißausbrüche, Atembeschwerden, Verdauungsbeschwerden, Flatulenz, Angst, Depression, Husten, Juckreiz und grippeähnliche Symptome.
ZUSAMMENFASSUNG
Mit Azidothymidin / Zidovudin (RETROVIR) steht erstmals eine Substanz zur kausalen Therapie der HIV-Infektion zur Verfügung. Es hemmt nach Phosphorylierung als falscher Baustein die
HI-Virus-Replikation in der Zelle. Es wirkt gegen die meisten Retroviren, also auch gegen die bisher bekannten HI-Viren Typ I und Typ II. Klinische Untersuchungen zeigten, daß sowohl die Häufigkeit
von ernsthaften sekundären Infektionen mit opportunistischen Erregern als auch die Letalität mit Azidothymidin gesenkt werden konnten. Allerdings treten relativ häufig Nebenwirkungen insbesondere mit
Schädigungen des Knochenmarkes auf. Solange noch keine Alternative zur Verfügung steht, sollten alle AIDS- und ARC-Patienten mit schweren Infektionen mit dieser Substanz behandelt werden. Die
optimale Dauer der Anwendung ist unbekannt, wahrscheinlich lebenslänglich.
Literatur
1. Informationen für den Arzt: RETROVIR.
Produktbeschreibung. Fa. Deutsche Wellcome GmbH, 1987
4. AZT Collaborative Working Group, 1987,
III. International Conference on AIDS T.8.4.
Ergänzungen
PubMed
Publikationen über Zidovudin mit den Stichworten
Ergänzungen
|
1. HIV Buch - ein umfangreiches Buch ist unter hivbuch.de kostenlos als PDF-Datei verfügbar.
2. Die Deutsche AIDS-Gesellschaft (DAIG) stellt auf ihrer Internetseite aktuelle Leitlinien und andere Informationen zur Verfügung.
|