Tipranavir - ein Proteaseinhibitor mit neuartiger Struktur
Unveränderter Text aus Heft 2, 2006
Aktuelle Ergänzungen am Ende des Textes
Das natürliche Substrat der HIV-spezifischen Protease ist ein Polyprotein, aus dem durch enzymatische Aktivität die viralen Proteine entstehen. Die bisher verfügbaren Proteaseinhibitoren (PI) sind
Peptid-ähnliche Moleküle, die aufgrund geringfügiger Modifikationen durch die Protease nicht gespalten werden können und damit das aktive Zentrum des Enzyms blockieren. Mit Tipranavir (APTIVUS) wurde
ein neuer Typ von Wirkstoffen gegen HIV entwickelt. [1,2] Es handelt sich um den ersten zur antiretroviralen Therapie zugelassenen nicht-peptidischen Protease-Inhibitor (NPPI). Die Substanz ist
indiziert bei mehrfach vorbehandelten Patienten mit Infektionen durch HIV-1-Viren, die gegen mehrere Protease-Hemmer resistent sind.
Antivirale Wirkung
Tipranavir hemmt die HIV-1 Aspartyl-Protease und unterdrückt die Reifung von Viruspartikeln in der Wirtszelle. In vitro hemmt Tipranavir die Replikation von HIV-1-Laborstämmen und klinischen Isolaten
in akuten T-Zell-Infektions-Modellen. Dabei lagen die wirksamen Konzentrationen (EC90) in einem Bereich von 0,07 bis 0,18 µM (42 – 108 ng/ml). Die antivirale Aktivität wird durch Humanserum etwa um
das 3- bis 4-fache reduziert. Von besonderem Interesse ist der Befund, dass dieser Proteaseinhibitor auch solche Stämme hemmt, die gegen die herkömmlichen Hemmstoffe der Protease resistent sind
[1,2].
Pharmakokinetische Eigenschaften
Die empfohlene tägliche Dosierung von Tipranavir beträgt 500 mg. Das Arzneimittel wird zweimal täglich in Form von Weichkapseln à 250 mg oral eingenommen. Um die geringe Bioverfügbarkeit zu
verbessern, wird Tipranavir mit 200 mg Ritonavir (NORVIR) kombiniert, dadurch resultieren mehr als 10fach höhere AUC-Werte im Vergleich zur alleinigen Einnahme. Die Plasmaspiegel von Ritonavir sind
bei gleichzeitiger Einnahme zusammen mit Tipranavir niedriger als bei alleiniger Gabe von Ritonavir. Daher ist die Dosis von Ritonavir doppelt so hoch wie bei anderen „geboosterten“
Proteaseinhibitoren (200 mg vs. 100 mg).
Die Einnahme zu einer Mahlzeit erhöht die Absorption und Verträglichkeit von Tipranavir. Die Spitzenkonzentration im Plasma wird in Abhängigkeit von der Dosis ein bis fünf Stunden nach der oralen
Einnahme erreicht. Bei wiederholter Einnahme ist die Plasmakonzentration geringer (ca. 85 µM). Als Ursache dafür wird eine Enzyminduktion in der Leber angenommen. Im Blut liegt Tipranavir zu über 90%
an Proteine gebunden vor. Der Arzneistoff wird größtenteils hepatisch über das Cytochrom P450-Enzymsystem, primär von dem Isoenzym CYP3A4, metabolisiert; Tipranavir ist auch ein Substrat des
Transportproteins P-Glykoprotein (P-gp). Die Ausscheidung erfolgt größtenteils unverändert mit den Faeces. Die mittlere Eliminations-Halbwertzeit von Tipranavir liegt bei etwa fünf bis sechs Stunden.
Bei Patienten mit mittelgradiger oder schwerer Leberinsuffizienz (Child-Pugh-Klasse B oder C) ist das Präparat kontraindiziert.
Interaktionen
Das Wechselwirkungsprofil von Tipranavir in Kombination mit Ritonavir ist sehr komplex3. Tipranavir induziert das P-gp und das Isoenzym CYP3A4, in Kombination mit Ritonavir wirkt es aber insgesamt
hemmend auf dieses Enzym. Wirkstoffe, die CYP3A und/oder p-GP induzieren, wie zum Beispiel Rifampicin (RIFA u.a.), können die Konzentration von Tipranavir herabsetzen und den therapeutischen Effekt
vermindern. Die gleichzeitige Behandlung mit Rifampicin ist daher kontraindiziert. Auch einige Statine, wie Lovastatin (MEVINACOR) und Simvastatin (ZOCOR u.a.), dürfen nicht gleichzeitig verabreicht
werden, die Anwendung von Atorvastatin (SORTIS) wird ebenfalls nicht empfohlen. Tipranavir/Ritonavir senken bei Gabe zusammen mit Nukleosidanaloga [Zidovudin (RETROVIR), Abacavir (ZIAGEN)] deren
Plasmakonzentration und können die Wirkung verringern. Eine Dosisanpassung wird aber nicht empfohlen. Bei der Kombination von Tipranavir mit nicht-nukleosidischen Reverse-Transkriptase-Hemmern
(NNRTI) [Nevirapin (VIRAMUNE), Efavirenz (SUSTIVA)] sollte vorsichtig vorgegangen werden. Die Gabe zusammen mit konventionellen Proteasehemmstoffen [Amprenavir (AGENERASE), Lopinavir (KALETRA),
Saquinavir (INVIRASE u.a.)] wird nicht empfohlen [3].
Die Kombination mit Midazolam i.v. (DORMICUM u.a.) führt zu einer verlängerten Halbwertzeit und zu erhöhten Plasmaspiegeln des Benzodiazepins. Clarithromycin (KLACID u.a.) führt zu einer veränderten
Pharmakokinetik von Tipranavir. Tipranavir/Ritonavir sollte nicht gemeinsam mit oralen Kontrazeptiva oder anderen östrogenhaltigen Arzneimitteln eingenommen werden. Weitere detaillierte Informationen
zu den bisher bekannten Interaktionen von Tipranavir/Ritonavir mit anderen Arzneimitteln sind über unsere Internetseite verfügbar (Interaktionen).
Therapeutische Wirksamkeit
Die Wirksamkeit und Verträglichkeit des neuen Arzneimittels wurde in zwei umfangreichen klinischen Studien untersucht. Die Studien sind unter dem Akronym RESIST (= Randomized Evaluation of Strategic
Intervention in multidrug reSistent patients with Tipranavir) bekannt geworden. Insgesamt konnten die Daten von fast 1200 Patienten ausgewertet werden, die alle bereits mehrfach mit antiretroviral
wirksamen Kombinationen behandelt worden waren. Eine Zwischenauswertung beider Studien nach 24 Wochen Therapie liegt vor und bildet die Basis der aktuellen Bewertung1. Danach war das neue
Arzneimittel signifikant besser wirksam als die bisher üblichen „geboosterten“ Proteaseinhibitoren. Die Ansprechraten, gemessen als Viruslast, lagen in der Tipranavir-Gruppe im Vergleich zur
Kontrollgruppe bei 42 vs. 22% (RESIST-1) und 41 vs. 15% (RESIST-2). Die Unterschiede waren in beiden Studien statistisch signifikant. Alle Patienten erhielten eine optimierte Kombinationstherapie;
den Fusionsinhibitor Enfuvirtid (FUZEON) bekamen 27% der Patienten in der Tipranavir-Gruppe und 22% in der Vergleichsgruppe. Bei Patienten mit HIV-Stämmen, die gegenüber den zum Vergleich
eingesetzten Proteaseinhibitoren empfindlich waren, konnte keine Überlegenheit des neuen Wirkstoffes gezeigt werden [1,2].
Unerwünschte Wirkungen
Die Verträglichkeit von Tipranavir in Kombination mit Ritonavir lässt sich anhand der Daten aus den RESIST-Studien abschätzen. Die Therapieabbruchrate lag bei den mit Tipranavir behandelten Patienten
bei 8% und damit doppelt so hoch, wie in der Vergleichsgruppe (4%) [1]. Als häufigste unerwünschte Wirkungen traten Diarrhö und Übelkeit auf. Hinzu kamen Kopfschmerz, Bauchschmerz und Hautausschläge.
Tipranavir in Kombination mit Ritonavir wird mit Fällen von signifikanter Lebertoxizität in Verbindung gebracht. Erhöhte Transaminasen waren unter Tipranavir häufiger als in der Vergleichsgruppe. Die
Patienten müssen deshalb engmaschig überwacht werden.
ZUSAMMENFASSUNG
Tipranavir (APTIVUS) ist ein neuer Proteaseinhibitor zur antiretroviralen Therapie. Die chemische Struktur der Substanz unterscheidet sich grundlegend von den bisher üblichen, peptidähnlichen
Proteaseinhibitoren, wie zum Beispiel Lopinavir (KALETRA). Die Aktivität gegen HIV-1 in vitro ist hoch, auch Viren mit Resistenz gegen die konventionellen Proteaseinhibitoren werden gehemmt. Um die
Bioverfügbarkeit zu verbessern, wird der Wirkstoff mit Ritonavir (NORVIR) in niedriger Dosierung kombiniert („geboostert“). Das Medikament wird zweimal täglich eingenommen. Die Elimination erfolgt
mit einer Halbwertzeit von etwa fünf bis sechs Stunden primär über die Leber. In zwei umfangreichen Phase-III-Studien wurde eine signifikante Überlegenheit des Präparates gegenüber herkömmlichen
Proteaseinhibitoren gezeigt. Die Verträglichkeit war im Vergleich zu den älteren Substanzen schlechter, was sich zum Beispiel in einer höheren Abbruchrate ausdrückte. Tipranavir stellt eine wichtige
Bereicherung der therapeutischen Möglichkeiten dar, wenn HIV-infizierte Patienten behandelt werden sollen, bei denen die konventionellen Proteaseinhibitoren nicht mehr wirksam
sind.
1. CROOM, K.F und
KEAM S.J. Tipranavir: a ritonavir-boosted protease inhibitor. Drugs 2005; 65:
1669 - 1677
2. Fachinfo APTIVUS, Boehringer Ingelheim (Okt. 2005)
3. BOFFITO, M. et
al. Practical
perspectives on the use of tipranavir in combination with other medications: lessons
learned from pharmacokinetic studies. J Clin Pharmacol 2006; 46: 130 – 139
Interaktion zwischen Proteaseinhibitoren und Loperamid
Loperamid (IMODIUM u.a.) wirkt als Agonist an peripheren Opioidrezeptoren und hemmt dadurch die Darmmotilität. Im ZNS
entfaltet es normalerweise keine Wirkungen, da es die Blut-Hirn-Schranke nicht überwindet. Dies wird durch einen Effluxmechanismus erreicht, der durch das Transportprotein P-gp (P-Glykoprotein)
vermittelt wird. Bei Durchfallerkrankungen ist Loperamid aufgrund seiner guten Wirksamkeit und Verträglichkeit ein lang bewährtes Medikament und wird auch bei Arzneimittel-bedingten Diarrhöen
empfohlen, die zum Beispiel im Zusammenhang mit der Einnahme von Proteaseinhibitoren auftreten können. Der Proteaseinhibitor Tipranavir (APTIVUS) wird zusammen mit Ritonavir (NORVIR) zur
antiretroviralen Therapie eingesetzt. Beide sind Substrate für P-gp und wirken als Induktor (Tipranavir) oder Inhibitor (Ritonavir) des Proteins. Angesichts der komplexen Situation lassen sich die zu
erwartenden Arzneimittelinteraktionen kaum voraussagen, wenn Tipranavir/Ritonavir zusammen mit Loperamid eingenommen wird. Zur Klärung dieser Situation wurde eine Interaktionsstudie bei 24
Freiwilligen durchgeführt, in der Plasmaspiegel und mögliche zentrale Nebenwirkungen von Loperamid erfasst wurden. Es zeigte sich, dass die Plasmaspiegel von Loperamid auf etwa das Doppelte
ansteigen, wenn das Antidiarrhoikum zusammen mit Ritonavir gegeben wird, anderseits resultieren deutlich niedrigere Spiegel bei gleichzeitiger Verabreichung von Tipranavir. Diese Reduktion wird nicht
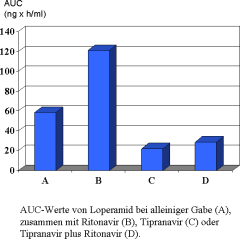
wesentlich verändert, wenn das Tipranavir „geboostert“ ist, also zusammen mit Ritonavir verabreicht wird. In der Abbildung werden die AUC-Werte (ng x h/ml) von Loperamid bei alleiniger Gabe und
zusammen mit den verschiedenen Komedikationen wiedergegeben.
Folgerung der Autoren
Bei gleichzeitiger Gabe des peripher wirksamen Opioids Loperamid (IMODIUM u.a.) und „geboostertem“ Tipranavir (APTIVUS) resultierte eine deutliche Senkung der Loperamid-Plasmaspiegel, es gab keine
Hinweise auf unerwünschte zentrale Wirkungen des Opioids. Wird der zur „Boosterung“ benutzte Wirkstoff Ritonavir (NORVIR) alleine mit Loperamid gegeben, resultieren dagegen deutlich erhöhte
Plasmaspiegel.
1. MUKWAYA, G. et
al. Interaction of ritonavir-boosted tipranavir with loperamide does not result in loperamide-associated neurologic side effects in healthy volunteers. Antimicrob
Agents Chemother 2005; 49: 4903 - 4910
Ergänzungen (Juli 2008)
Seit der Erstellung und Veröffentlichung dieses Artikels in der
Zeitschrift für Chemotherapie (Heft 2, 2006) sind zahlreiche weitere Arbeiten über Tipranavir publiziert worden. Insbesondere soll an dieser Stelle auf die folgenden Arbeiten hingewiesen
werden:
1. GATHE J. et
al. Efficacy of the Protease Inhibitors Tipranavir plus Ritonavir in Treatment-Experienced Patients:
24-Week Analysis from the RESIST-1 Trial Clin Infect
Dis 2006; 43: 1337-1346
2. CAHN P. et
al. Ritonavir-Boosted Tipranavir Demonstrates Superior Efficacy to
Ritonavir-Boosted Protease
Inhibitors in Treatment-Experienced HIV-Infected Patients: 24-Week Results of the RESIST-2 Trial Clin Infect
Dis 2006; 43: 1347-1356
3. ORMAN JS, PERRY
CM. Tipranavir: A
Review of its Use in the Management of HIV Infection. Drugs.
2008;68(10):1435-63.