Ribavirin - in Kombination mit Interferon wirksam bei Hepatitis C
Aktuelle Ergänzungen am Ende des Textes
Ribavirin (REBETOL) wurde bereits 1972 erstmals beschrieben. In vitro besitzt es Aktivität gegen RNA- und DNA-Viren.1 Ende der achtziger Jahre erfolgte die Zulassung des
Nukleosid-Analogons als Aerosol zur Therapie von RS-Virusinfektionen bei Kindern. Für diese Indikation ist es als VIRAZOLE im Handel. Als orale Zubereitungsform wird es in Kombination mit Interferon a (INTRON A, ROFERON A) erfolgreich zur Therapie der Hepatitis C eingesetzt. Während die Monotherapie
mit Ribavirin nicht erfolgreich ist, ist der Effekt des Interferons bei kombinierter Gabe signifikant verbessert. Der Mechanismus, durch den das Nukleosid seine Wirkung auf das Hepatitis C-Virus in
Kombination mit Interferon entfaltet, ist unbekannt. Erwachsene Patienten mit chronischer Hepatitis C erhalten in Kombination mit Interferon a (3 mal wöchentlich 3 Mio IE) täglich entweder 1000 mg
(<75 kg) oder 1200 mg (>75 kg) Ribavirin aufgeteilt in zwei Tagesdosen. Die Dauer der Therapie liegt je nach viralem Genotyp und anderen prognostischen Faktoren bei 24 bis 48
Wochen.2
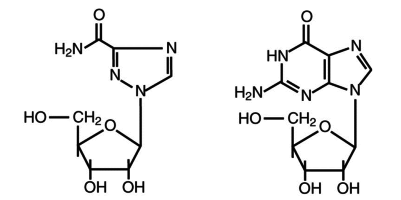
Ribavirin Guanosin
Strukturformel Ribavirin. Das Virustatikum ist ein Guanosin-Analogon, das nach intrazellulärer Phosphorylierung die Guanosintriphosphat-Synthese hemmt. Es ist in vitro gegen mehrere DNA- und RNA-Viren aktiv.
Pharmakokinetische Eigenschaften
Eine Einzeldosis Ribavirin wird nach oraler Gabe rasch resorbiert und mit einer Halbwertzeit von etwa
80 Stunden eliminiert. Die absolute Bioverfügbarkeit wird mit 45 bis 65% angegeben. Die Kinetik unterliegt einer hohen inter- und intraindividuellen Variabilität, die teilweise durch einen
ausgeprägten first-pass Metabolismus erklärt werden kann. Das Nukleosid-Analogon wird nicht an Plasmaproteine gebunden, das scheinbare Verteilungsvolumen wurde mit 5000 l berechnet. Ribavirin wird
über spezielle Nukleosidtransporter in Erythrozyten und andere Zellen transportiert. Das Verhältnis zwischen den Konzentrationen von Ribavirin im Vollblut und Plasma beträgt etwa 60. Der überwiegende
Teil des Ribavirins im Blut liegt in Form von Nukleotiden in Erythrozyten vor. Nach Abspaltung des Riboserestes und weiteren metabolischen Schritten entsteht ein Triazolcarbonsäure-Metabolit, der
renal eliminiert wird.
Bei mehrfacher Einnahme kumuliert die Substanz. Bei Einnahme von 2 x täglich 600 mg wurde ein „steady state“ mit Plasmakonzentrationen von 2,2 µg/ml nach etwa 4 Wochen erreicht. Nach Absetzen der
Therapie betrug die Halbwertzeit ca. 300 Stunden, was wahrscheinlich durch die langsame Freisetzung aus den Nicht-Plasma-Kompartimenten erklärt werden kann. Die Bioverfügbarkeit wird durch eine
gleichzeitig eingenommene, fettreiche Mahlzeit deutlich erhöht; es wird daher empfohlen, das Präparat zusammen mit der Nahrung einzunehmen. Bei Patienten mit eingeschränkter Nierenfunktion waren
AUC-Werte und Spitzenkonzentrationen von Ribavirin erhöht, bei eingeschränkter Leberfunktion wurden dagegen keine Veränderungen festgestellt. Patienten mit einer Kreatininclearance von < 50 ml/min
dürfen nicht mit Ribavirin behandelt werden.
Über Interaktionen zwischen Ribavirin und anderen Arzneimitteln ist wenig bekannt, eine geringe, klinisch nicht relevante Reduktion der Resorption erfolgt bei Einnahme mit Antazida. Die Substanz
hemmt nicht die Cytochrom-abhängigen Monooxygenasen – entsprechende Wechselwirkungen sind daher unwahrscheinlich.
Unerwünschte Wirkungen, Toxizität
Bei bis zu 14% der Patienten, die im Rahmen klinischer Studien mit der Kombination aus Ribavirin und Interferon behandelt wurden, kam es zu einer Abnahme
des Hämoglobin-Spiegels auf < 10 g/dl und anderen Blutbildveränderungen. Als Folge der Anämie muß mit einer Verschlechterung der Symptomatik bei Patienten mit kardialen Erkrankungen gerechnet
werden. Des weiteren kommt es zu Reaktionen von seiten des Magen-Darm-Traktes (Übelkeit, Anorexie), neurotoxischen Symptomen (Schlaflosigkeit, Reizbarkeit), Hautveränderungen (Pruritus, Exanthem,
Hauttrockenheit) und Schilddrüsenfunktions-störungen. Eine Dosisreduktion oder Unterbrechung der Therapie aufgrund von unerwünschten Wirkungen war bei bis zu 21% der Patienten, die mit der
Kombination behandelt wurden, erforderlich.
Im Tierexperiment führte Ribavirin bei niedrigen Dosierungen zu Veränderungen der Spermien und erwies sich als embryotoxisch bzw. teratogen. Frauen im gebärfähigen Alter müssen während und bis zu 4
Monate nach der Therapie zuverlässige kontrazeptive Maßnahmen durchführen. Während dieser Zeit muß monatlich routinemäßig ein Schwangerschaftstest durchgeführt werden.
ZUSAMMENFASSUNG
Die Kombinationstherapie der Hepatitis C mit Interferon a (INTRON A, ROFERON A) plus Ribavirin (REBETOL) ist besser wirksam
als die Gabe von Interferon alleine und stellt einen wichtigen Fortschritt in der Hepatitistherapie dar. Angesichts der erheblichen unerwünschten Wirkungen, die bei dieser Behandlung auftreten
können, sollte die Therapie spezialisierten Ärzten vorbehalten sein.
1. KUCERS A. et al. The use of antibiotics, 5th ed., Butterworth – Heinemann, S. 1812
2. Fachinformation REBETOL, Essex Pharma
Ergänzung (2006)
Seit der Erstellung und Veröffentlichung dieses Artikels in der Zeitschrift für Chemotherapie (Heft 3, 1993) sind zahlreiche weitere Arbeiten über Ribavirin publiziert worden. Insbesondere soll an dieser Stelle auf die folgenden Arbeiten hingewiesen werden:
1. TOVO PA, LAZIER L et al. Hepatitis B virus and hepatitis C virus
infections in children. Curr Opin Infect Dis. 2005
Jun;18(3):261-6.
2. SIEBERT U, SROCZYNSKI G et al. Effectiveness and cost-effectiveness of
initial combination therapy with interferon/peginterferon plus
ribavirin in patients with chronic hepatitis C in Germany: a health technology assessment commissioned by the German Federal Ministry of Health and
Social Security. Int J Technol Assess Health Care. 2005
Winter;21(1):55-65.
3. KEATING GM, PLOSKER GL. Peginterferon alpha-2a (40KD) plus ribavirin: a
review of its use in the management of patients with chronic hepatitis
C and persistently 'normal' ALT levels. Drugs.
2005;65(4):521-36.
4. TRIANTOS C, SAMONAKIS D Liver transplantation and hepatitis C virus:
systematic review of antiviral therapy. Transplantation. 2005 Feb
15;79(3):261-8.
5. KOWDLEY KV. Hematologic side effects of interferon and ribavirin
therapy. J Clin Gastroenterol. 2005 Jan;39(1 Suppl):S3-8.
6. PLOSKER GL, KEATING GM. Peginterferon-alpha-2a (40kD) plus ribavirin: a
review of its use in hepatitis C Virus And HIV co-infection. Drugs.
2004;64(24):2823-43.
7. HOOFNAGLE JH, SEEFF LB. Peginterferon and Ribavirin for chronic hepatitis C. N. Engl J Med 2006; 355:2444-2451.
Ergänzung (2017)
Interferon-Ribavirin-Kombination nicht mehr üblich bei Hepatitis C
Interferon-freie Therapieoptionen mit direkt wirkenden Virustatika stellen heute den Therapiestandard für die chronische Hepatitis dar. Im Vergleich zu Interferon-basierten Therapieschemata sind sie überlegen und führen zu einer dauerhaften Viruseradikation („sustained virologic response“, SVR). Das gilt für praktisch alle HCV-Genotypen und Therapiekonstellationen. Ribavirin, dessen antiviraler Wirkungsmechanismus bis heute nicht genau bekannt ist, spielt in verschiedenen antiviralen Regimen als Kombinationspartner weiterhin eine gewisse Rolle.