Nadifloxacin - irrationaler Einsatz eines Fluorchinolons zur lokalen Aknetherapie
Fluorchinolone gehören seit zwei Jahrzehnten zu den unverzichtbaren Arzneimitteln bei bakteriellen Infektionen. Die zunehmende Verschlechterung der Resistenzsituation wird allerdings weltweit als ein wichtiges Problem angesehen. Eine vorrangige Maßnahme ist in diesem Zusammenhang ohne Zweifel die restriktive Verordnung von Antiinfektiva und die Beschränkung der Chinolontherapie auf gut begründete Indikationen. Vor diesem Hintergrund muss die Einführung einer Cremezubereitung zur lokalen Therapie der Akne als irrational eingestuft werden. Die Creme enthält den Wirkstoff Nadifloxacin in einer Konzentration von 1%. Als Indikationen für die äußerliche Anwendung werden „leichte bis mittelschwere Ausprägungen entzündlicher Formen der Akne vulgaris“ angegeben. Das Arzneimittel ist bereits seit dem Jahr 2000 zugelassen, es wurde vor einigen Monaten in Deutschland unter dem Handelsnamen NADIXA in den Handel gebracht. [1]
Antibakterielle Aktivität, Resistenz
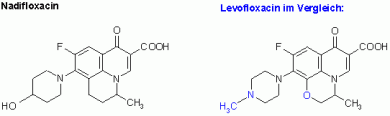
Ein Blick auf die Formel des „neuen Aknewirkstoffes“ Nadifloxacin und ein Vergleich mit der Struktur von Ofloxacin (TARIVID, OFLOHEXAL u.a.) bzw. Levofloxacin (TAVANIC) zeigt die nahe chemische Verwandtschaft der
Substanzen.
Strukturformel Nadifloxacin
(Unterschiede zu Levofloxacin sind blau markiert)
Vergleichsuntersuchungen belegen, dass Nadifloxacin zum Beispiel eine sehr ähnliche Aktivität wie Levofloxacin gegen Pneumokokken und P. acnes aufweist, bei Staphylokokken ist es deutlich aktiver.
Von besonderem Interesse ist angesichts der Indikation ein Vergleich der inhibitorischen Konzentrationen von Nadifloxacin und Erythromycin (AKNEMYCIN SALBE u.a.), das ebenfalls zur topischen
Aknetherapie angeboten wird, gegen Propionibacterium acnes. Nadifloxacin war in vitro gegen die pathogenetisch wichtige Bakterienspezies deutlich schwächer wirksam als das Makrolid: die MHK50-Werte
lagen bei 0,39 mg/L (Nadifloxacin) und 0,05 mg/L (Erythromycin). [2]
Seit etwa 30 Jahren haben die Dermatologen bereits Erfahrungen mit lokal angewandten Antibiotika in der Aknetherapie gesammelt. Mit allen Antibiotika erwies sich die Resistenzentwicklung von P. acnes
als wichtigstes Problem. Entsprechende Daten für Nadifloxacin bei längerer und häufiger Anwendung wurden bisher nicht publiziert. Im direkten Vergleich über zehn Wochen war in der Resistenzlage von
P. acnes kein Unterschied zu Erythromycin erkennbar, bei Koagulase-negativen Staphylokokken zeigten sich mit Nadifloxacin tendenziell günstigere Resultate. [3] In der topischen Antibiotikatherapie
der Akne spielt neben Erythromycin heute nur noch Clindamycin (BASOCIN AKNE GEL) eine Rolle, Tetrazykline und Chloramphenicol werden kaum noch verwandt. Generell wird Zurückhaltung bei der lokalen
Antibiotikatherapie gefordert. Stattdessen wird zur Behandlung das unspezifisch antibakteriell wirksame Benzoylperoxid (PANOXYL u.a.) als Mittel der Wahl angesehen, da es mit dieser Substanz keine
entsprechenden Resistenzprobleme gibt. [4]
In der Werbung für NADIXA wird es als „das erste topische Chinolon in der Akne-Therapie“ bezeichnet. Jedem Arzt sollte jedoch klar sein, dass es keine „topischen Chinolone“ geben kann, sondern dass
alle Chinolone unabhängig von der Applikationsart ihre Wirkung durch Hemmung der bakteriellen Topoisomerasen II und IV entfalten. Damit besteht zwischen den einzelnen Wirkstoffen dieser wichtigen
Arzneimittelgruppe die Möglichkeit für die Entwicklung von Kreuzresistenzen und durch die häufige therapeutische Verwendung entsteht ein erheblicher Selektionsdruck. Es kann erwartet werden, dass
durch die neue Indikation „Akne“ eine weitere Ausbreitung der Chinolon-Resistenz resultiert.
Pharmakokinetik, unerwünschte Wirkungen
Die Resorption des Wirkstoffes durch die Haut ist gering, bei Patienten mit geschädigter Haut, wie es bei Aknepatienten
der Fall ist, gelangt jedoch eine größere Menge des Chinolons ins Blut. Die Plasmakonzentrationen können Werte von etwa 1 bis 3 ng/ml erreichen. Die Metabolisierung von Nadifloxacin erfolgt über
Oxidations- und Konjugationsreaktionen; es wird unverändert und in metabolisierter Form mit den Fäces und über die Nieren ausgeschieden. [1]
Während der Behandlung mit NADIXA-Creme können Hautreizungen auftreten. Bei nicht indizierter, mehrmals täglicher Applikation sind eine ausgeprägte Rötung und ein unangenehmes Gefühl auf der Haut
möglich. Als unerwünschte Wirkungen sind auch Juckreiz und Wärmegefühl, Kontaktdermatitis und Urticaria beobachtet worden. Vereinzelt wurde über Hypopigmentierung der Haut berichtet. [1]
Nadifloxacin ist keineswegs ein „neues“ Chinolon. Die ersten Veröffentlichungen über die breite antibakterielle Aktivität der Substanz mit der Kurzbezeichnung OPC-7251 erschienen bereits in den
1980er Jahren. Ähnlich wie Ofloxacin liegt Nadifloxacin als Racemat vor. Neben den antibakteriellen Eigenschaften der Substanz fanden auch die genotoxischen Effekte des Arzneistoffes besonderes
Interesse bei japanischen Wissenschaftlern während der präklinischen Entwicklung der Substanz.5 Heute wird in der Fachinfo des Präparates darauf hingewiesen, dass „Konzentrationen mit genotoxischen
Effekten“ therapeutisch nicht erreicht werden.
ZUSAMMENFASSUNG
In Form einer Hautcreme wird das Fluorchinolon Nadifloxacin (NADIXA) zur Therapie der Akne vulgaris in den Handel gebracht. Der Wirkstoff weist eine ähnliche Struktur und ein ähnliches antibakterielles Spektrum wie Levofloxacin (TAVANIC) auf, eine Förderung von Kreuzresistenzen ist bei breiter Anwendung zu befürchten. Die wichtigsten unerwünschten Wirkungen betreffen die Haut (Erythem, Juckreiz, Kontaktdermatitis etc.). Da zur Aknetherapie zahlreiche andere, bewährte Wirkstoffe zur Verfügung stehen [z. B. Benzoylperoxid (PANOXYL u.a.)], muss das neue Präparat nicht nur als überflüssig, sondern sogar als eine bedenkliche Neuentwicklung im Angebot der Chinolone angesehen werden.
1. FACHINFO NADIXA®, Ferrer Internacional, Barcelona, Vertrieb: Dr. R. Pfleger, Bamberg
2. YAMAKAWA T, MITSUYAMA J et al. In vitro and in vivo antibacterial activity of T-3912, a novel non-fluorinated topical quinolone. J Antimicrob Chemother. 2002 Mar;49(3):455-65.
3. GOLLNICK, H. et al.
Eur J Dermatol 1994; 4: 210 - 215
4. GOLLNICK
HP, KRAUTHEIM A. Topical
treatment in acne: current status and future aspects. Dermatology.
2003;206(1):29-36.
5. TAKAHASHI
N, SHIRAGIKU T et al. In
vitro clastogenicity of optical isomers of nadifloxacin. Arzneimittelforschung.
1994 Nov;44(11):1265-8.