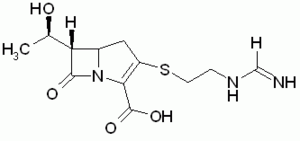
Imipenem / Cilastatin - ein ß-Laktam-Antibiotikum mit breitem Spektrum
Unveränderter Text aus ZCT Heft 3, 1985
Ergänzungen am Ende des Textes
Imipenem / Cilastatin (ZIENAM) ist ein neues, von der Firma MSD Sharp & Dohme GmbH, USA, entwickeltes ß-Laktam-Antibiotikum zur parenteralen Therapie von bakteriellen Infektionen. Es besteht aus
dem Hauptwirkungspartner Imipenem, welches mit Cilastatin-Natrium - einer antibiotisch nicht aktiven Substanz - kombiniert wurde, um den metabolischen Abbau von Imipenem in der Niere zu
verhindern.
Wie wir in der Zeitschrift für Chemotherapie (ZCT 1984, Heft 6,
1984, S. 45-46) mitteilten, hatte das Bundesgesund-heitsamt am 5. Oktober 1984 das "Ruhen der Zulassung" für Imipenem angeordnet. Die damalige Begründung beruhte vorwiegend auf vermeintlich hohen
Todesfallzahlen unter der Behandlung mit dem Chemotherapeutikum, welche sich jedoch seit den ersten klinischen Prüfungen im Prinzip unverändert zwischen 4,3 und 5,0% der zumeist schwerkranken
Patienten bewegten. Mit einigen, noch zu erwähnenden Änderungen im Beipackzettel wurde das Arzneimittel zum 1. April 1985 nun wieder voll zugelassen. Insgesamt kann die sechs Monate dauernde
"Ruheaktion" des BGA nicht als adäquat eingestuft werden; es bleibt abzuwarten, inwieweit sich dieser Vorgang auf die Akzeptanz dieses Antibiotikums auswirken wird.
Mikrobiologie
Imipinem ist das erste stabile ß-Laktam-Antibiotikum
aus der Gruppe der Thienamycine (sogenannte Carbapeneme). Es unterscheidet sich in seiner chemischen Struktur wesentlich von Penicillinen und Cephalosporinen: Das Schwefelatom im Thiazolring der
Penicilline ist durch ein Kohlenstoffatom ersetzt, und die Seitenkette ist an den ß-Laktamring in trans-Konfiguration gebunden. Imipenem wirkt wie alle ß-Laktam-Antibiotika auf die Hemmung der
Zellwandbiosynthese der Bakterien (Penicillin-bindende Proteine). An über 14.000 Isolaten konnte gezeigt werden, daß das antibakterielle Spektrum des Imipenem den gramnegativen und grampositiven
Bereich umfaßt. E. coli, Klebsiellen, Enterobacter, Citrobacter, Salmonellen, Shigellen, Pseudomonas species, Haemophilus influenzae, Neisserien, Yersinien und die gramnegativen Anaerobier
(Bacteroides species, Fusobakterien) werden in niedrigen Konzentrationen gehemmt. Staphylokokken, Pneumokokken, hämolysierende Streptokokken und Enterokokken (insb. Streptococcus faecalis) sind
ebenfalls hochempfindlich, gleichfalls auch Peptostreptokokken. Pseudomonas maltophila und Pseudomonas cepacia werden nicht ausreichend erfaßt. Imipenem besitzt eine höhere ß-Laktamasestabilität als
z.B. Cefotaxim (CLAFORAN).
Der Kombinationspartner Cilastatin hat keine eigene antibiotische Aktivität und beeinflußt auch nicht die antibakterielle Wirkung von Imipenem. Cilastatin bewirkt zwei Effekte:
- Reduzierung der Hydrolyse von Imipenem in der Niere und damit Erhöhung der Imipenem-Urinspiegel sowie
- die Verhinderung einer bei Kaninchen und Affen beobachteten Nephrotoxizität des Antibiotikums in sehr hoher Dosierung.
Pharmakokinetik
Die pharmakokinetischen Daten der beiden
Kombinationspartner stimmen gut überein. Bei einem üblichen Mischungsverhältnis von 1:1 werden nach jeweils 500 mg i.v. maximale Serumspiegel von im Mittel 33 mg/l bzw. nach 1000 mg mittlere
Spitzenspiegel von 66 mg/l gemessen. Die Halbwertzeit beider Substanzen beträgt 50-60 min, die totale Körperclearance liegt im Mittel bei 190 ml/min. Die renale Clearance des Imipenem bei
kombinierter Gabe wird mit 138 ml/min angegeben, die des Cilastatin liegt geringfügig niedriger. Innerhalb von 24 Stunden lassen sich 72% des verabreichten Imipenem im Urin nachweisen. In der
Kombination sind die Serumspiegel gegenüber der Einzelgabe geringfügig erhöht. Die Proteinbindung beider Substanzen liegt im Serum bei 25%, die Verteilungsvolumina bewegen sich zwischen 8 und 15
l.
Von Bedeutung ist die unterschiedlich ausgeprägte Halbwertzeitverlängerung beider Kombinationspartner bei verschiedenen Graden der Niereninsuffizienz. So verlängert sich die Halbwertzeit von Imipenem
bei mittelgradiger Niereninsuffizienz (Glomerulumfiltrat von 15-30 ml/min) auf 127±28 min, während Cilastatin bei diesem Grad der Nierenfunktionseinschränkung mit einer Halbwertzeit von 150±60 min
ausgeschieden wird. Bei einem Glomerulumfiltrat von weniger als 15 ml/min sind die Parameter noch deutlicher unterschiedlich (159±18 min für Imipenem und fast 400±94 min für Cilastatin). Es empfiehlt
sich daher unbedingt eine deutliche Dosisreduktion schon bei einem Glomerulumfiltrat von unter 30 ml/min, um eine Kumulation der Substanzen - insbesondere des Cilastatin - zu
vermeiden.
Klinik
Die klinischen Ergebnisse mit dem neuen Präparat sind als recht günstig zu bewerten. So liegen die entsprechenden Heilungsquoten zwischen 74 und 92% bei der klinischen Beurteilung. Diese Zahlen sind mit anderen modernen ß-Laktam-Antibiotika vergleichbar. Infektionen der Atemwege, der Harnwege, des Abdomens, der Haut sowie Wundinfektionen, Septikämien, gynäkologische sowie Gelenk- und Knocheninfektionen wurden mit ZIENAM erfolgreich behandelt. Zumeist handelte es sich um fortgeschrittene bakterielle Infektionen bei Patienten mit schweren Grunderkrankungen.
Verträglichkeit
Die Daten zur Verträglichkeit und Sicherheit, wie sie inzwischen bei fast 4000 Patienten weltweit erfaßt wurden, liegen in der Größenordnung anderer neuerer ß-Laktam-Antibiotika. Im Vordergrund der Unverträglichkeitsreaktionen stehen lokale Neben wirkungen (Phlebitis 5%), gefolgt von gastrointestinalen Symptomen (4,5%). Bei den intestinalen Unverträglich-keitsreaktionen sind auch pseudo-membranöse Kolitiden beobachtet worden. Gelegentlich wurde über Superinfektionen mit Candida berichtet.
Ein Behandlungsabbruch wegen Nebenwirkungen war zwischen 0,8 und 4,9% erforderlich. Relativ auffällig ist die hohe Zahl von Thrombophlebitiden bei peripher-venöser Applikation; unter den Laborparametern fielen mäßig erhöhte, jedoch durchweg reversible Leberfunktionswerte auf (alk. Phosphatase, SGOT, SGPT).
Probleme bereiten dem BGA offensichtlich die in knapp 1% aufgetretenen ZNS-Reaktionen, die jedoch auch bei anderen
ß-Laktam-Antibiotika gelegentlich beobachtet werden. Immerhin sah sich die Zulassungsbehörde veranlaßt, im Beipackzettel einen Warnhinweis für Patienten mit bereits bestehenden Störungen des ZNS zu
verlangen.
ZUSAMMENFASSENDE BEWERTUNG
Imipenem/Cilastatin (ZIENAM) ist ein ß-Laktam-Antibiotikum, welches aufgrund seiner hohen Aktivität und seines Spektrums in vielen Fällen in Monotherapie - also z.B. ohne gleichzeitige Gabe eines Aminoglykosids - eingesetzt werden kann. Das kann als ein therapeutischer Fortschritt angesehen werden. Das Thienamycinderivat sollte jedoch unbedingt Patienten mit schweren bzw. lebensbedrohlichen Infektionen vorbehalten werden. Die tägliche Dosierung dürfte bei normaler Nierenfunktion mit 2 g ausreichend sein; bei einem Glomerulumfiltrat von weniger als 30 ml/min muß die Dosis reduziert werden. Bei Patienten mit cerebralen Vorschädigungen, insbesondere in hohem Alter und bei bestehender Niereninsuffizienz, sollte die Substanz nur bei dringlicher Indikation eingesetzt werden.
Ergänzung (2000)
Literatur zu Imipenem
Seit seiner Einführung im Jahre 1985 hat sich Imipenem als erstes Carbapenem zur parenteralen antibiotischen Therapie in
der Klinik bewährt. Seit der Erstellung und Veröffentlichung dieses Artikels in der Zeitschrift für Chemotherapie (Heft 3, 1985) sind zahlreiche weitere Arbeiten über Imipenem publiziert worden.
Insbesondere soll an dieser Stelle auf die folgenden Übersichtsarbeiten hingewiesen werden:
Asbel LE, Levison ME. Cephalosporins, carbapenems, and monobactams. Infect Dis Clin North Am. 2000;14:435-447
Ergänzung (2009)
Übersicht Carbapeneme
Weitere Carbapeneme - wie Meropenem, Doripenem und Ertapenem - sind nach der Einführung des Imipenem in den Handel gekommen. Ein Übersichtsartikel zu den pharmakologischen Grundlagen und zur klinischen Wirksamkeit der Carbapeneme erschien im Heft 4, 2009 (PDF-Datei) dieser Zeitschrift.
Ergänzung (2019)
Leitlinie der PEG
Auf die ausführliche PEG S2k Leitlinie (AWMF-Registernummer 082-006) der Paul-Ehrlich-Gesellschaft für Chemotherapie e.v. (PEG) Kalkulierte parenterale Initialtherapie bakterieller Erkrankungen bei Erwachsenen – update 2018 (2. aktualisierte Version; 25. Juli 2019) sei an dieser Stelle hingewiesen.
Link zum download der PDF-Datei