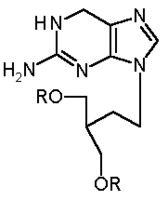
Famciclovir - ein neues Virustatikum zur Behandlung von Herpes-Infektionen
Unveränderter Text aus ZCT Heft 2, 1995
Ergänzungen am Ende des
Textes
Penciclovir ist ein neu entwickeltes Nukleosid-Analogon mit antiviralen Eigenschaften. Die Bioverfügbarkeit dieses neuen Wirkstoffes ist jedoch nicht ausreichend, um ihn zur oralen Therapie
einzusetzen. Daher wurde Famciclovir (FAMVIR), ein Prodrug des Wirkstoffes, entwickelt, der sich durch gute pharmakokinetische Eigenschaften auszeichnet und seit einigen Wochen nun auch in
Deutschland zur Behandlung von Herpes-Infektionen angeboten wird.
Antivirale Eigenschaften
Zum antiviralen Spektrum von Penciclovir gehören in erster Linie das Varizella-Zoster-Virus, Herpes
simplex-Virus Typ 1 und Typ 2 und das Epstein-Barr-Virus. Auch gegenüber Zytomegalie-Viren und Hepatitis B-Viren ist die Verbindung in vitro wirksam.
Penciclovir wird in Virus-infizierten Zellen durch die virale Thymidinkinase in das entsprechende Penciclovir-Monophosphat umgewandelt. Anschließend erfolgt intrazellulär in weiteren
Phosphorylierungsschritten die Umwandlung in das Triphosphat, welches den eigentlichen Wirkstoff darstellt. Penciclovir-Triphosphat hemmt kompetitiv die virale DNA-Polymerase und führt nach Einbau in
die DNA zum Kettenabbruch. Das antiviral wirksame Triphosphat besitzt in Zellen, die mit dem Varizella-Zoster-Virus infiziert sind, eine intrazelluläre Halbwertzeit von etwa 9 Stunden.
Der molekulare Wirkungsmechanismus des Penciclovir ist also mit dem Mechanismus von Aciclovir (ZOVIRAX u.a.) und anderen Nukleosid-Analoga vergleichbar und im Prinzip identisch, doch zeichnet sich
das biologisch aktive Triphosphat durch eine deutlich längere (ca. 10fache) intrazelluläre Halbwertzeit aus.[1]
Pharmakokinetische Eigenschaften
Da Penciclovir nicht in ausreichendem Maße aus dem Gastrointestinaltrakt resorbiert wird, ist Famciclovir entwickelt worden, aus dem im Organismus Penciclovir entsteht. Chemisch gesehen ist es das Diacetyl-5-deoxy-Analog des Penciclovir. Die Abspaltung der beiden Acetylreste sowie die Oxidation des Moleküls erfolgen rasch, so daß der Arzneistoff nach oraler Gabe des Medikamentes im Plasma oder Urin nicht, oder nur in sehr geringen Konzentrationen, nachweisbar ist.
Die Bioverfügbarkeit von Famciclovir wurde mit 77% errechnet. Die Spitzenspiegel von Penciclovir werden nach etwa 45 Minuten erreicht, die Substanz wird mit einer Halbwertzeit von etwa 2 Stunden überwiegend renal eliminiert. Die Spitzenkonzentration nach Einnahme von 250 mg liegt bei 1,6 mg/l und die "Fläche unter der Konzentrations-Zeit-Kurve" wurde mit 4,3 mg x h/l berechnet. In einem Dosisbereich von 125 bis 750 mg Famciclovir verändern sich die pharmakokinetischen Parameter linear.[2]
Bei gleichzeitiger Verabreichung des Chemotherapeutikums mit einer Mahlzeit ergab sich keine signifikante Veränderung der Bioverfügbarkeit. Die Spitzenkonzentration im Plasma war zwar niedriger als bei nüchterner Einnahme, doch waren die AUC-Werte nicht signifikant unterschiedlich.
Interaktionen
In mehreren Studien an gesunden Probanden wurde überprüft, ob Famciclovir zu klinisch relevanten Interaktionen mit anderen gleichzeitig gegebenen Arzneimitteln führt. In diesem Zusammenhang muß bedacht werden, daß Famciclovir nicht nur durch Esterhydrolyse, sondern auch durch oxidative Schritte in den eigentlichen Wirkstoff umgewandelt werden muß. Da die Möglichkeit diskutiert wurde, daß das Enzym Xanthinoxidase an dieser Umwandlung beteiligt sei, wurde zunächst eine Interaktionsstudie mit Allopurinol (ZYLORIC u.a.) - einem Hemmstoff der Xanthinoxidase - durchgeführt; es ergab sich kein Anhalt auf eine relevante Beeinflussung der Pharmakokinetik von Famciclovir durch das Urikostatikum. Zu ähnlichen Resultaten führten weitere Interaktionsstudien mit Cimetidin (TAGAMET u.a.), Theophyllin (EUPHYLLIN u.a.) und Digoxin (LANICOR u.a.). In keinem Fall konnte eine relevante Interaktion festgestellt werden.[3]
Therapeutische Wirksamkeit
In doppelblind durchgeführten klinischen Studien zur Therapie des akuten Herpes zoster bei immunkompetenten Patienten erwies sich die Behandlung mit 3 x 250 mg Famciclovir pro Tag hinsichtlich der Verkürzung der Hautsymptomatik als ebenso wirksam wie die tägliche Behandlung mit 5 x 800 mg Aciclovir.[4] Auch die Gabe von Famciclovir muß möglichst rasch nach Auftreten der Symptomatik erfolgen (< 72 Stunden). Im Vergleich mit Aciclovir waren die mit Famciclovir behandelten Patienten signifikant schneller schmerzfrei, wenn die Therapie innerhalb von 48 Stunden nach Auftreten der Hautsymptome begonnen wurde. Die Frage, ob das neue Virustatikum einen positiven Effekt auf die Entwicklung postherpetischer Schmerzen hat, kann zur Zeit noch nicht abschließend beurteilt werden.
Unerwünschte Wirkungen
Während einer Doppelblindstudie erwies sich Famciclovir als ebenso gut verträglich wie Aciclovir. Am
häufigsten wurden gastrointestinale Störungen und ZNS-Reaktionen gesehen. Die Gesamtrate der "unerwünschten Erscheinungen", die während dieser Untersuchung beobachtet wurden, lag bei 22%
(Famciclovir) bzw. 21% (Aciclovir) der Patienten. Diese Angaben beinhalten auch jene Reaktionen, die hinsichtlich des kausalen Zusammenhanges mit dem jeweiligen Medikament nicht beurteilt werden
konnten.[4]
ZUSAMMENFASSUNG
Famciclovir (FAMVIR) wird im Organismus zu Penciclovir metabolisiert. Dieses Nukleosid-Analogon wirkt
nach weiterer Umwandlung zum Triphosphat virustatisch. Da das Medikament eine deutlich bessere Bioverfügbarkeit besitzt als Aciclovir (ZOVIRAX u.a.) und der Wirkstoff intrazellulär eine wesentlich
längere Verweildauer aufweist, kann das neue Arzneimittel in relativ niedriger Dosierung verabreicht werden (3 x täglich 250 mg). In klinischen Vergleichsstudien bei immunkompetenten Patienten mit
Zoster war eine entsprechende Behandlung mindestens ebenso wirksam und gleich gut verträglich, wie die Behandlung mit 5 x 800 mg Aciclovir.
Entscheidend ist jedoch bei beiden Medikamenten ein rascher Behandlungsbeginn. Weitere Studien werden derzeit weltweit durchgeführt, um die Indikationen für Famciclovir zu erweitern. Daher kann der
genaue Stellenwert des neuen Virustatikums zur Therapie von Infektionen durch Herpes-Viren noch nicht abschließend beschrieben werden. Ganz sicher stellt es jedoch eine interessante Alternative zum
Aciclovir bei Patienten mit Zoster dar.
1. HODGE RA, PERKINS RM. Mode of action of 9-(4-hydroxy-3-hydroxymethylbut-1-yl)guanine (BRL 9123) against herpes simplex virus in MRC-5 cells. Antimicrob Agents Chemother 1989 Feb;33(2):223-9.
2 PUE, M.A., BENET, L.Z.
Antiviral Chem. & Chemother. 4 (Suppl): 47-55, 1993
3. DANIELS, S., SCHENTAG, J.J.
Antiviral Chem. & Chemother. 4 (Suppl): 57-64, 1993
4. DEGREEF, H. et al.,
Int. J. Antimicrob. Agents 4: 241-246, 1994
Ergänzung (2008)
Seit der Erstellung und Veröffentlichung dieses Artikels in der Zeitschrift für Chemotherapie (Heft 2, 1995) sind zahlreiche
weitere Arbeiten über Famciclovir publiziert worden. Insbesondere soll an dieser Stelle auf die folgenden Arbeiten hingewiesen werden:
PERRY CM, WAGSTAFF AJ.
Famciclovir. A review of its pharmacological properties and therapeutic efficacy in herpesvirus infections. Drugs. 1995 Aug;50(2):396-415.
SACKS SL, AOKI FY et al.
Patient-initiated, twice-daily oral famciclovir for early recurrent genital herpes. A randomized, double-blind multicenter trial. JAMA. 1996 Jul 3;276(1):44-9.
ALRAHBI FA, SACKS SL. New
antiherpesvirus agents. Their targets and therapeutic potential. Drugs. 1996 Jul;52(1):17-32.
FARO S. A review of famciclovir
in the management of genital herpes. Infect Dis Obstet Gynecol.
1998;6(1):38-43.
SACKS SL. Famciclovir
suppression of asymptomatic and symptomatic recurrent anogenital herpes simplex virus shedding in women: a randomized, double-blind, double-dummy, placebo-controlled, parallel-group, single-center
trial. J Infect Dis. 2004 Apr 15;189(8):1341-7.
Sacks SL, Aoki FY et al.
Clinic-initiated, twice-daily oral famciclovir for treatment of recurrent genital herpes: a randomized, double-blind, controlled trial. Clin Infect Dis. 2005 Oct 15;41(8):1097-104.
SIMPSON D, LYSENG-WILLIAMSON KA. Famciclovir: a review of
its use in herpes zoster and genital and orolabial herpes. Drugs. 2006;66(18):2397-416.
DWORKIN RH, JOHNSON RW et al. Recommendations for the management of herpes zoster. Clin Infect Dis. 2007 Jan 1;44 Suppl 1:S1-26.
Ergänzung (2018)
Herpes zoster - neue Erkenntnisse
Eine Übersicht mit dem Titel „Herpes zoster - neue Erkenntnisse zu Epidemiologie, Pathogenese, Therapie und Prävention“ finden Sie im Heft 4, 2008 dieser Zeitschrift.
Ergänzung (2018)
Impfprophylaxe des Herpes zoster
Unter dem Handelsnamen SHINGRIX ist eine Subunit-Vakzine zur Prophylaxe des Herpes zoster im Handel. Sie enthält das rekombinante Antigen E, ein wesentliches Glykoprotein des Virus und ein speziell entwickeltes Adjuvans. In Placebo-kontrollierten klinischen Studien konnte die Wirksamkeit des Impfstoffes nachgewiesen werden. Sie liegt bei über 90% und zwar in allen Altersgruppen von 50- bis zu über 80-jährigen Patienten.