Elbasvir / Grazoprevir - eine Kombination aus zwei neuen Wirkstoffen zur Therapie der Hepatitis C
Unveränderter Text aus Heft 1, 2017
In rascher Folge sind in den vergangenen Jahren neue Medikamente zur Behandlung der chronischen Hepatitis C in den Handel gekommen. Therapeutika, die noch vor wenigen Jahren als Fortschritt galten, sind heute bereits obsolet. Die Bemühungen um fixe Kombinationen, die nur einmal täglich genommen werden müssen, haben zu einem weiteren Präparat mit zwei neuen Inhaltsstoffen geführt. Unter dem Namen ZEPATIER ist seit kurzem eine Kombination aus dem NS3/4A-Proteaseinhibitor Grazoprevir und dem NS5A-Hemmer Elbasvir zur Behandlung der Hepatitis C im Handel. Da die Wirksamkeit der Kombination bei den HCV-Genotypen 2, 3, 5 und 6 nicht gezeigt wurde, wird die Anwendung bei mit diesen Genotypen infizierten Patienten nicht empfohlen.1
Antivirale Aktivität
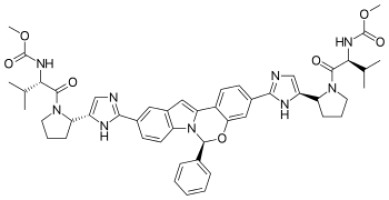
Elbasvir ist bereits der vierte therapeutisch verfügbare Inhibitor des NS5A-Replikationskomplexes. Die Wirkstoffe dieser Gruppe hemmen die Viren bereits bei sehr geringen Konzentrationen, die Resistenzbarriere ist allerdings eher niedrig. Mit Elbasvir wurde eine optimierte Substanz mit hoher antiviraler Potenz entwickelt. Es handelt sich um ein tetrazyklisches Indolderivat.2
Strukturformel Elbasvir (MK-8742; MM 882 g/mol)
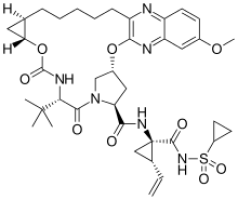
Während der Entwicklung von Grazoprevir wurde gezielt nach Varianten gesucht, mit denen sich auch in der Leber relativ hohe Konzentrationen erreichen lassen und die auch gegen resistente Viren Aktivität zeigen.3 Grazoprevir wirkt auch gegen die klinisch relevanten Mutanten mit Veränderungen in der R155, A156 oder D168 Position. Der Arzneistoff ist in vitro aktiv gegen die Genotypen 1 bis 6 des Hepatitis C-Virus. Um eine ausreichende Wirksamkeit bei Infektionen mit dem Genotyp 3 zu erreichen, sind allerdings höhere Dosierungen notwendig, die mit hepatotoxischen Reaktionen assoziiert waren.4
Strukturformel Grazoprevir (MK-5172; MM 766,9 g/mol)
Pharmakokinetische Eigenschaften
Elbasvir und Grazoprevir werden nach oraler Gabe ausreichend resorbiert. Im Vergleich zur Nüchterneinnahme sind bei der Einnahme mit einer fettreichen Mahlzeit die Plasmakonzentrationen von Elbasvir reduziert und die von Grazoprevir erhöht. Diese Veränderungen werden als nicht klinisch relevant angesehen, so dass das Arzneimittel unabhängig von der Nahrungsaufnahme eingenommen werden kann. Beide Wirkstoffe sind in hohem Maße (> 99,9 % bzw. 98,8 %) an humane Plasmaproteine gebunden. Sie werden zum Teil mittels oxidativer Metabolisierung eliminiert, hauptsächlich durch CYP3A. Die terminale Halbwertzeit beträgt etwa 24 Stunden für Elbasvir (50 mg) und ungefähr 31 Stunden für Grazoprevir (100 mg). Beide Komponenten werden mit dem Stuhl eliminiert.
Klinische Studien
In den klinischen Studien wurden auch Patienten behandelt, bei denen wegen einer fortgeschrittenen Niereninsuffizienz oder aus anderen Gründen die Therapieresultate mit den bisherigen Arzneimitteln nicht optimal waren.
Bei nicht vorbehandelten Patienten, bei denen eine Infektion mit einem der drei Genotypen 1, 4 oder 6 vorlag, konnte eine anhaltende Virusfreiheit nach zwölfwöchiger Behandlung (SVR12) zu 95% erreicht werden (Studie: C-EDGE TN, treatment naive). Auch bei insgesamt 420 bisher erfolglos mit Peginterferon und Ribavirin Vorbehandelten (Studie: C-EDGE TE, treatment experienced) wurde anhaltende Virusfreiheit (SVR12) bei 92 bis 97% der Patienten erzielt. Weder eine längere Therapiedauer von 16 Wochen (anstatt 12 Wochen) noch die Zugabe von Ribavirin (diverse Generika) beeinflusste das Ergebnis.5
In der C-SURFER-Studie wurden Patienten mit HCV-Infektion Genotyp-1 und fortgeschrittener Niereninsuffizienz behandelt (GFR < 30 ml/min), etwa 80% der Teilnehmer waren dialysepflichtig. Fast alle Patienten erreichten die SVR12, nur bei einem Patienten wurde in der Nachuntersuchung ein virologischer Rückfall festgestellt.6
Schließlich widmete sich die C-SALVAGE-Studie einer Gruppe von Patienten, die bereits mit einem Protease-Inhibitor plus Ribavirin plus Peginterferon alpha vorbehandelt worden waren. Bei diesen Patienten wurde das Kombinationspräparat zusammen mit Ribavirin gegeben. Auch bei diesen Patienten wurde eine anhaltende Beseitigung der Viren bei 96% der Teilnehmer erreicht.7
Verträglichkeit, Interaktionen
Die Verträglichkeit des Kombinationspräparates in klinischen Studien war gut. Unterschiede zu den Placebo-behandelten Gruppen wurden nicht registriert, spezifische Nebenwirkungen wurden nicht beobachtet.
Elbasvir und Grazoprevir hemmen im Darm den Arzneimitteltransporter BCRP, was zu einem Anstieg der Plasmakonzentrationen von Atorvastatin (diverse Generika) und anderen Statinen führen kann. Elbasvir zeigt keine Hemmung des Cytochrom-Enzyms CYP3A, mit Grazoprevir wurde dagegen eine schwache Inhibition von CYP3A gezeigt. Die Dosierung von CYP3A-Substraten muss bei gleichzeitiger Anwendung mit ZEPATIER nicht angepasst werden. Die gleichzeitige Anwendung von CYP-Induktoren, wie Carbamazepin (diverse Generika), ist kontraindiziert, da eine Abnahme der Konzentrationen der Virustatika zu erwarten ist.
ZUSAMMENFASSUNG
Mit dem neuen Kombinationspräparat ZEPATIER werden bei Patienten mit chronischer Hepatitis C hohe Heilungsraten erzielt. Das Arzneimittel enthält die bisher nicht verfügbaren Wirkstoffe Elbasvir (ein NS5A-Inhibitor) und den Protease-Inhibitor Grazoprevir in fixer Kombination. Die guten Therapieerfolge konnten in den umfangreichen klinischen Studien auch bei Patienten mit relativ schlechter Prognose nachgewiesen werden. Das Präparat ist gut verträglich, potenzielle Interaktionen mit einigen Arzneistoffen müssen beachtet werden.
1. SPC Zepatier (Produktinformation)