Doripenem - ein Carbapenem zur parenteralen Therapie schwerer Infektionen
Unveränderter Text aus Heft 5, 2008
Ergänzungen am Ende des Textes
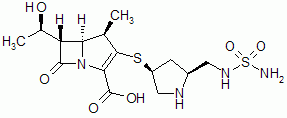
Thienamycin - der Vorläufer der Carbapeneme - wurde Mitte der 1970er Jahre aus Streptomyces cattleya isoliert. Die Bezeichnung „cattleya“ für diese Streptomycesart wurde gewählt, weil die Kulturen des Mikroorganismus farblich an Orchideenblüten der Gattung Cattleya erinnern. [1] Thienamycin ist aufgrund seiner Instabilität nicht als Arzneimittel geeignet, daher ist der Naturstoff durch chemische Modifikationen kontinuierlich weiter entwickelt worden. Während das klassische Imipenem (ZIENAM) nur zusammen mit Cilastatin als „Stabilisator“ angewandt werden konnte, sind mit Meropenem (MERONEM) und Ertapenem (INVANZ) mittlerweile auch zwei Carbapeneme erhältlich, die nicht durch Dehydropeptidasen in der menschlichen Niere abgebaut werden. Mit Doripenem (DORIBAX) steht nun ein weiteres Carbapenem zur Verfügung, das für die Behandlung von schweren, oft lebensbedrohlichen Infektionen zugelassen ist. Auch dieses Molekül weist eine 1-ß-Methylgruppe am Grundgerüst auf (s. Abbildung), die der Substanz Stabilität gegenüber einer Hydrolyse durch die Dehydropeptidase verleiht.[2,3]
Der Pfeil markiert die 1-ß-Methylgruppe, die der Substanz Stabilität gegenüber der Dehydropeptidase verleiht.
Antimikrobielle Aktivität
Die charakteristische Eigenschaft der Carbapeneme ist ihr breites antibakterielles Wirkungsspektrum gegen grampositive und gramnegative, aerobe und anaerobe Bakterien. [4] Doripenem ist im grampositiven Bereich etwa so wirksam wie Imipenem und gegen gramnegative Bakterien etwa so wirksam wie Meropenem. Nicht zum Spektrum gehören Methicillin-resistente Staphylokokken und E. faecalis. Bemerkenswert ist vor allem die verbesserte Aktivität gegen Pseudomonas aeruginosa. Alle während einer klinischen Studie bei beatmeten Patienten mit nosokomialer Pneumonie isolierten Stämme von P. aeruginosa wurden durch Konzentrationen von höchstens 4 mg Doripenem / l gehemmt; dies traf bei Imipenem nur auf 19 von 25 Stämmen zu, bei drei Stämmen wurde eine MHK von 8 mg/l und bei weiteren drei Stämmen eine MHK von ≥16 mg/l bestimmt. [5] Von Interesse ist auch die hohe Aktivität gegen Acinetobacter baumannii und andere Erreger, die ß-Laktamasen mit erweitertem Spektrum bilden (ESBL).
Pharmakokinetische Eigenschaften
Doripenem wird in einer Dosierung von 500 mg alle acht Stunden über eine Stunde infundiert; aufgrund
der relativ hohen Stabilität bei Raumtemperatur ist mit Doripenem auch eine verlängerte Infusion bis zu vier Stunden möglich. Dadurch verlängert sich die Zeit, in denen die Plasmaspiegel von
Doripenem über der MHK der jeweiligen Erreger liegen. Die „Zeit über der MHK“ ist der entscheidende pharmakologische Parameter für die bakterizide Wirkung der ß-Laktamantibiotika. Die längere
Infusionsdauer kann gerade bei komplizierten Infektionen geeignet sein, da auch weniger empfindliche Erreger erfasst werden können. Nach einstündiger Infusion lag die Spitzenkonzentration im Plasma
bei 23 mg/l, der AUC-Wert wurde mit 36 mg/l x h berechnet. [2,6]
Doripenem verteilt sich gut in Körperflüssigkeiten und Geweben, die Plasmaproteinbindung ist mit ca. 8,1% niedrig. Das Carbapenem wird durch Öffnung des ß-Laktamringes zu einem mikrobiologisch
inaktiven Metaboliten hydrolysiert. Doripenem wird vorwiegend unverändert über die Nieren ausgeschieden; ca. 20% lassen sich im Urin in Form des Metaboliten nachweisen. Die mittlere
Eliminations-Halbwertzeit aus dem Plasma bei gesunden Erwachsenen ist kurz, sie beträgt etwa eine Stunde; für den Metaboliten wurde eine Eliminationshalbwertzeit von 2,5 Stunden ermittelt.6 Bei
Personen über 66 Jahre ist die AUC etwa 50% höher als bei jüngeren Probanden. Dies ist in erster Linie auf eine geringere Kreatinin-Clearance (CrCl) im Alter zurückzuführen.
Bei Patienten mit mäßigen bis schweren Störungen der Nierenfunktion ist in Abhängigkeit von der Kreatinin-Clearance eine Dosisreduktion und/oder eine Verlängerung des Applikationsintervalls
erforderlich.Bei einer Kreatinin-Clearance von 30 bis 50 ml/ min soll die Dosierung halbiert werden (250 mg alle acht Stunden), bei einer CrCl < 30 ml/ min wird diese reduzierte Dosis nur alle 12
Stunden infundiert. [2]
Klinische Wirksamkeit
Die klinische Wirksamkeit von Doripenem bei nosokomialen Pneumonien wurde in zwei offenen Studien an
insgesamt 979 Patienten überprüft (DORI-09, DORI-10). Doripenem erwies sich dabei als mindestens gleich gut wirksam wie die Vergleichsantibiotika Imipenem oder Piperacillin / Tazobactam (TAZOBAC). Die klinischen Heilungsraten der 531
beatmeten Patienten in der DORI-10 Studie lagen bei 68% (Doripenem) und 64% (Imipenem), ein größerer Unterschied war bei Infektionen durch P. aeruginosa erkennbar: hier betrug die Heilungsrate unter
Doripenem 80% (16 von 20 Patienten) und unter Imipenem 42,9% (6 von 14 Patienten), der Unterschied war jedoch nicht statistisch signifikant.5 Die mittlere Krankenhaus-Verweildauer war in dieser
Studie unter Doripenem mit 22 Tagen signifikant kürzer als unter Imipenem mit 27 Tagen (p=0,01). Patienten in der Doripenem-Gruppe mussten nur sieben Tage beatmet werden, die Beatmungsdauer in der
Imipenem-Gruppe lag dagegen bei zehn Tagen (p=0,034). Die Liegedauer auf der Intensivstation war in beiden Gruppen vergleichbar. [7]
In zwei Doppelblindstudien wurden 946 erwachsene Patienten mit komplizierten intraabdominellen Infektionen mit Doripenem (500 mg i.v. über eine Stunde alle acht Stunden) oder Meropenem (1.000 mg i.v.
Bolus-Injektion alle acht Stunden) behandelt. Nach mindestens drei Tagen parenteraler Therapie war ein Wechsel auf eine orale Behandlung mit Coamoxiclav (AUGMENTAN u.a.) erlaubt. Doripenem war sowohl
nach klinischen als auch nach mikrobiologischen Kriterien vergleichbar gut wirksam wie Meropenem. Die Heilungsraten lagen jeweils bei ca. 85%. [8]
In zwei weiteren Studien wurden die Wirksamkeit und Verträglichkeit von Doripenem bei Patienten mit komplizierten Harnwegsinfektionen einschließlich Pyelonephritis überprüft. In einer
Doppelblindstudie wurden die Patienten zum Vergleich mit Levofloxacin (TAVANIC, 250 mg alle 24 Stunden) behandelt. Die Behandlung dauerte zehn Tage mit der Option, auf eine orale Levofloxacin-Therapie nach mindestens drei Tagen i.v.-Therapie zu
wechseln. Doripenem erwies sich auch bei dieser Indikation als nicht-unterlegen gegenüber Levofloxacin hinsichtlich mikrobiologischer Eradikationsraten oder der klinischen Heilungsrate.
[9]
Unerwünschte Wirkungen, Interaktionen
In den klinischen Studien wurde Doripenem gut vertragen. Als unerwünschte Wirkungen wurden am
häufigsten Kopfschmerzen (10 %), Diarrhö (9 %) und Übelkeit (8 %) registriert. Ferner traten Pruritus, Hautausschlag, Phlebitis, orale Candidose, Pilzinfektionen der Vulva und Erhöhungen der
Leberenzyme auf. Krampfauslösende Wirkungen wurden nur sehr selten beobachtet. Nur bei 0,1% der Patienten kam es zu einem Nebenwirkungs-bedingten Abbruch der Therapie. [2]
Bei gleichzeitiger Gabe von Valproinsäure (ERGENYL u.a.) mit Meropenem oder anderen Carbapenemen sind die Plasmakonzentrationen des Antiepileptikums deutlich reduziert und es kann zu Krampfanfällen
kommen. [10,11] Valproinsäure wird überwiegend durch Glukuronidierung verstoffwechselt, der Metabolit wird anschließend teilweise aber auch wieder hydrolytisch gespalten. Offenbar hemmen die
Carbapeneme die Hydrolyse des Glukuronids und dadurch liegt weniger freie Valproinsäure im Plasma vor. Die Serumspiegel von Valproinsäure müssen daher kontrolliert und die Dosierung eventuell
angepasst werden, wenn Doripenem oder ein anderes Carbapenem gleichzeitig verabreicht wird.
Zusammenfassung
Mit Doripenem (DORIBAX) steht ein neues Carbapenem zur parenteralen Therapie schwerer Infektionen zur Verfügung. Das
Antibiotikum ist in vitro aktiv gegen ein breites Spektrum grampositiver und gramnegativer, aerober und anaerober Bakterien einschließlich Pseudomonas und ESBL-Bildner. Die übliche Dosis von 500 mg
wird dreimal täglich als Infusion über eine Stunde verabreicht. Aufgrund seiner guten Stabilität in wässrigen Lösungen kann es auch über vier Stunden infundiert werden. Die Elimination erfolgt mit
einer Halbwertzeit von etwa einer Stunde renal, bei Niereninsuffizienz muss die Dosis reduziert werden. In umfangreichen, teils doppelblind durchgeführten klinischen Prüfungen erwies es sich als
wirksam bei Patienten mit nosokomialen Pneumonien, einschließlich Pneumonien bei beatmeten Patienten, sowie bei komplizierten abdominellen Infektionen und komplizierten Harnwegsinfektionen
einschließlich Pyelonephritis. Das Antibiotikum war gut verträglich. Bei gleichzeitiger Gabe von Valproinsäure (ERGENYL u.a.) müssen die Spiegel des Antiepileptikums kontrolliert werden, da mit
Interaktionen aufgrund der Erfahrungen mit anderen Carbapenemen gerechnet werden muss.
1. KAHAN JS, KAHAN FM et al. Thienamycin, a
new beta-lactam antibiotic. I. Discovery, taxonomy, isolation and physical properties. J Antibiot (Tokyo).
1979 Jan;32(1):1-12.
2. Doribax Fachinfo, Janssen-Cilag, Stand: 07 / 2008
3. ZHANEL GG, WIEBE R et al. Comparative
review of the carbapenems. Drugs. 2007;67(7):1027-52.
4. GE Y, WIKLER MA et al. In
vitro antimicrobial activity of doripenem, a new carbapenem. Antimicrob Agents Chemother. 2004
Apr;48(4):1384-96.
5. CHASTRE J, WUNDERINCK R et
al. Efficacy and safety of intravenous infusion of doripenem versus imipenem in ventilator-associated
pneumonia: a multicenter, randomized study. Crit Care Med. 2008
Apr;36(4):1089-96.
6. CIRILLO I, MANNENS G et al.
Disposition, metabolism, and excretion of [14C]doripenem after a single 500-milligram intravenous infusion in
healthy men. Antimicrob
Agents Chemother. 2008;52(10):3478-83.
7. MERCHANT S, GAST C et al.
Hospital resource utilization with doripenem versus imipenem in the treatment of
ventilator-associated pneumonia. Cliin Ther. 2008; 30: 717 -
33.
8. LUCASTI C, JASOVICH A et al.
Efficacy and tolerability of IV doripenem versus meropenem in adults with complicated intra-abdominal
infection: a phase III, prospective, multicenter, randomized, double-blind, noninferiority study. Clin Ther.
2008;30(5):868-83.
9. NABER, K. et al. ECCMID 2007, München, Poster 833
10. NAKAJIMA Y, MIZOBUCHI M et al.
Mechanism of the drug interaction between valproic acid and carbapenem antibiotics in monkeys and rats. Drug
Metab Dispos. 2004; 32(12):1383-91.
11. NACARKUCUK E, SAGLAM H et
al. Meropenem decreases serum level of
valproic acid. Pediatr
Neurol. 2004;31(3):232-4.
Ergänzung 2012
Rote Hand Brief DORIBAX
Aktuelle Studien haben gezeigt, dass eine Dosierung von 500 mg alle 8 Stunden nicht für alle Patienten mit nosokomialer Pneumonie ausreicht. Die Firma Janssen empfiehlt, bei der Behandlung mit Doripenem von Patienten mit nosokomialer Pneumonie und insbesondere bei Infektionen mit gramnegativen Erregern wie Pseudomonas aeruginosa und Acinetobacter spp. sowohl die Therapiedauer zu verlängern als auch die Dosis zu erhöhen. Rote Hand Brief DORIBAX
Ergänzung 2014
Einstellung des Vertriebs in der EU
Der Vertrieb des Arzneimittels DORIBAX (Doripenem) wurde im März 2014 in Europa eingestellt. Die Rechte an DORIBAX wurden von der Firma Janssen an seinen Lizenzpartner Shionogi zurück übertragen. Shionogi hat entschieden, die Vermartung des Antibiotikums in der EU einzustellen. Mitteilung der EMA