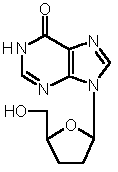
Didanosin - ein neues Nukleosid-Analogon zur Behandlung der HIV-Infektion
Unveränderter Text aus ZCT Heft 6, 1992
Aktuelle Ergänzungen am Ende des Textes
Didanosin (VIDEX) ist ein neu zugelassenes Nukleosid-Derivat, das in vitro und in vivo gegen das HI-Virus wirksam ist1.
Neben Zidovudin (RETROVIR) steht damit ein zweites Arzneimittel aus dieser Wirkstoff-Gruppe zur Therapie der HIV-Infektion zur Verfügung. Beide haben
positive Wirkungen auf verschiedene Marker der Infektion, doch sind sie nicht in der Lage, die Virusinfektion zu heilen - sie verlangsamen nur das Fortschreiten der Erkrankung.
Strukturformel Didanosin.
Antivirale Wirkung
In vitro-Untersuchungen zeigten, daß Didanosin (= 2',3'-Dideoxyinosin, DDI) bei Konzentrationen, die unter therapeutischen Bedingungen erreichbar sind, zu einer Hemmung der Replikation von HIV führt. Diese Konzentration liegt etwa bei 20 µmol/l und verursacht keine allgemeine Zytotoxizität; insbesondere zeigte die Verbindung - im Gegensatz zu Zidovudin - nur geringe Wirkungen auf Stammzellen des Knochenmarks. Nach der Diffusion von Didanosin in die Zelle wird die Substanz zu Didesoxyadenosintriphosphat (ddATP) umgewandelt, welches das physiologische Substrat dATP verdrängt und wahrscheinlich die biologisch aktive Form des Virustatikums darstellt. In vitro konnte ein synergistischer antiviraler Effekt mit Zidovudin oder Ribavirin (in Deutschland nicht im Handel) festgestellt werden. Es bestand keine Kreuzresistenz zu Zidovudin-resistenten Viren. Bei langfristiger Exposition gegenüber Didanosin ist eine Abnahme der Empfindlichkeit von HIV beobachtet worden.
Pharmakokinetische Eigenschaften
Im sauren Milieu des Magens ist Didanosin nicht stabil. Die Arzneizubereitung enthält
deshalb Zusätze, die als Puffer wirken oder die Substanz muß zusammen mit Antazida eingenommen werden. Unter diesen Bedingungen liegt die Bioverfügbarkeit bei etwa 40%, die Variabilität ist jedoch
erheblich. Die Einnahme muß auf nüchternen Magen erfolgen. Wenn zuvor der H2-Blocker Ranitidin (ZANTIC, SOSTRIL) gegeben wird, ist die Bioverfügbarkeit geringfügig höher (Anstieg der AUC-Werte um
14%), andere pharmakokinetische Parameter werden nicht beeinflußt2. Etwa eine halbe Stunde nach der Gabe von 10 mg Didanosin/kg KG wurden bei AIDS-Patienten maximale Plasmakonzentrationen von 24
µmol/l gemessen. Die Substanz wird mit einer Halbwertzeit von etwa einer Stunde ausgeschieden. Das biologisch wirksame Triphosphat wird aus den Zellen jedoch langsamer eliminiert (HWZ: ca. 12
Stunden).
Endprodukte des Metabolismus sind Didesoxyadenosintriphosphat, Harnsäure und andere Purinmetabolite. Ein erheblicher Teil einer verabreichten Dosis
erscheint in unveränderter Form im Urin. Bei Patienten mit eingeschränkter Nierenfunktion ist die Halbwertzeit auf das Dreifache verlängert, durch Dialyse wird Didanosin aus dem Plasma
entfernt.
Klinische Wirksamkeit
In Phase I- und Phase II/III-Studien wurde ein positiver Effekt des Chemotherapeutikums auf Marker der HIV-Infektion
(Anzahl der CD4-positiven Zellen, CD4/CD8-Verhältnis, p24-Antigen etc.) beobachtet. Über die Ergebnisse einer Vergleichsstudie zwischen Zidovudin und Didanosin an fast 1.000 Patienten haben wir
bereits in der letzten Ausgabe dieser Zeitschrift ausführlich berichtet (ZCT 13: 36, 1992). Es konnten zwar leichte Vorteile bei Behandlung mit 500 mg nachgewiesen werden, enttäuschend war jedoch die
Tatsache, daß kein signifikanter Unterschied in der Mortalität zwischen den Gruppen erkennbar war.
Weitere klinische Studien sind notwendig, um die Wirksamkeit des Medikamentes in früheren Stadien der HIV-Infektion zu überprüfen - insbesondere auch in Kombination mit anderen Medikamenten, wie zum
Beispiel Zidovudin oder Interferon alpha (ROFERON u.a.).
Unerwünschte Wirkungen
Die wichtigsten Therapie-limitierenden unerwünschten Wirkungen während der Phase I-Untersuchungen waren periphere Neuropathie und Pankreatitis (9% der Patienten). Die Inzidenz einer tödlich verlaufenden Pankreatitis wird als Ergebnis von Phase II-Studien an über 10.000 Patienten mit 0,35% angegeben. Das Risiko für diese schwerwiegende Nebenwirkung scheint bei fortgeschrittenem Stadium der Infektion sowie bei Einnahme anderer Medikamente oder bei gleichzeitigem Alkoholkonsum erhöht zu sein. Zahlreiche andere unerwünschte Wirkungen sind beobachtet worden (z.B. Hepatitis, Optikusneuritis, Exantheme, Kopfschmerzen, Schlaflosigkeit), doch ist naturgemäß die Kausalität der Symptome nur schwer zu belegen, da bei HIV-Patienten im fortgeschrittenen Stadium der Erkrankung viele Symptome auch krankheitsbedingt sein können.
ZUSAMMENFASSUNG:
Mit Didanosin (VIDEX) steht neben Zidovudin (RETROVIR) ein weiteres Virustatikum aus der Gruppe der Nukleoside zur Behandlung von HIV-Patienten zur Verfügung. Es hemmt die Vermehrung des AIDS-Erregers in vitro und in vivo. Bei mässiger Bioverfügbarkeit nach oraler Gabe wird das Medikament sowohl renal unverändert eliminiert als auch metabolisiert. Sorgfältig durchgeführte klinische Studien müssen abgewartet werden, um für diese Medikamente klar definierte Indikationen zu benennen. Da sie sich hinsichtlich des Nebenwirkungspotentials unterscheiden, kommen sie bei Unverträglichkeitsreaktionen als gegenseitige Alternative in Betracht. Auch bei Resistenzentwicklung der Viren unter der Therapie besteht nun die Möglichkeit, das Chemotherapeutikum zu wechseln. So ergeben sich neue therapeutische Alternativen, jedoch keine grundsätzlich neuen Aspekte in der Behandlung von AIDS-Patienten.
Literatur:
1: FAULDS, D., Brogden, R.N.
Drugs 44: 94-116, 1992
2: KNUPP, C. et al. Antimicrob.
Agents Chemother. 36: 2075-2079, 1992
Ergänzung (Juli 2008)
Seit der Erstellung und Veröffentlichung dieses Artikels in der Zeitschrift für Chemotherapie (Heft 6, 1992) sind zahlreiche weitere Arbeiten über Didanosin publiziert worden. Insbesondere soll an dieser Stelle auf die folgenden Arbeiten hingewiesen werden:
Perry, C.M. et al. Drugs.
1996; 52: 928-962.
Carpenter, C.C.J. et al. JAMA. 1998; 280: 78-86
MORENO S,
HERNANDEZ B et al. Didanosine enteric-coated capsule:
current role in patients with HIV-1 infection.
Drugs. 2007;67(10):1441-62.
Ergänzung (2014)
|
1. Ein umfangreiches ständig aktualisiertes Buch ist unter hivbuch.de kostenlos als PDF-Datei verfügbar.
2. Die Deutsche AIDS-Gesellschaft (DAIG) stellt auf ihrer Internetseite aktuelle Leitlinien und andere Informationen zur Verfügung.
|
Ergänzung (2019)
Der Hersteller Bristol-Myers Squibb teilt mit, dass der Vertrieb des Präparates VIDEX (Didanosin) eingestellt wird. In den Leitlinien wird das Nukleosid-Analogon bereits seit längerem nicht mehr zur Behandlung der HIV-Infektion empfohlen. Es stehen Alternativen mit einem besseren Nutzen-Risiko-Verhältnis zur Verfügung.