Dalbavancin – ein neues Glykopeptid zur Behandlung von Haut- und Weichgewebeinfektionen
Unveränderter Text aus ZCT Heft 5, 2015
Ergänzungen am Ende des Textes
Die Gruppe der Glykopeptid-Antibiotika ist in den vergangenen Monaten mehrfach erweitert worden. Nach Telavancin (VIBATIV) sind mit Dalbavancin (XYDALBA) und Oritavancin (ORBACTIV) zwei halbsynthetische Antibiotika aus dieser Gruppe zugelassen worden, die sich durch ihre lange Halbwertzeit auszeichnen. Ungewöhnlich ist, dass sich die einzelnen Glykopeptide – trotz ähnlicher antibakterieller Aktivität – auch in ihren Indikationsgebieten deutlich unterscheiden. Während die beiden älteren Glykopeptide Vancomycin (diverse Generika) und Teicoplanin (TARGOCID) für die Behandlung einer Reihe von unterschiedlichen Indikationen zugelassen sind, ist die Zulassung von Telavancin auf die Therapie von ambulant und nosokomial erworbenen Pneumonien begrenzt. Auch die lang wirksamen Präparate sind nicht breit anwendbar: Dalbavancin und Oritavancin sind nur für die Behandlung von Haut- und Weichgewebeinfektionen verfügbar.
Die Entwicklung von Dalbavancin verlief eher langsam, was angesichts der hohen antibakteriellen Aktivität erstaunlich ist. Erste Daten über das Wirkungsspektrum des Antibiotikums – damals noch unter der Bezeichnung BI397 oder A-A-1 - wurden bereits in den 1990er Jahren publiziert.1 Ein erster Zulassungsantrag unter dem Handelsnamen EXULETT wurde bei der EMEA 2008 gestellt. Die klinischen Studien überzeugten das zuständige Komitee (CHMP) jedoch nicht, so dass der Zulassungsantrag zurückgezogen wurde. Im Dezember 2014 erfolgte dann die Empfehlung zur Zulassung des Antibiotikums unter dem Handelsnamen XYDALBA durch das CHMP.2
Herkunft, chemische Struktur
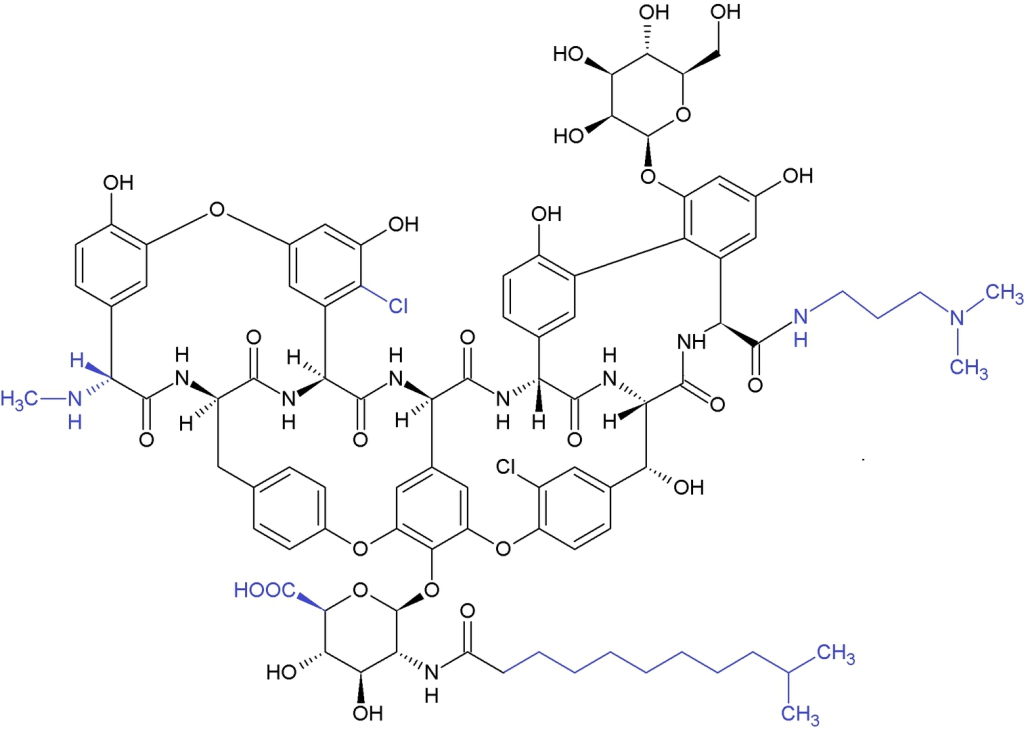
Dalbavancin wird halbsynthetisch aus dem natürlich vorkommenden Glykopeptid A-40926 hergestellt, das strukturell mit Teicoplanin verwandt ist. Ähnlich wie Teicoplanin handelt es sich um ein Gemisch von Verbindungen, die sich geringfügig in dem lipophilen Substituenten unterscheiden, wobei die B0-Komponente den weitaus größten Anteil (>75%) ausmacht. Die lipophile Substitution ist charakteristisch für Dalbavancin, das daher auch als Lipoglykopeptid bezeichnet wird.3
Strukturformel von Dalbavancin (B0-Komponente). Es besitzt eine ähnliche Struktur wie andere Glykopeptide. Dalbavancin ist ein Heptapeptid mit kovalenter Verbrückung der phenolischen Seitenketten. Die Unterschiede zu Teicoplanin sind blau markiert (z. B. längere lipophile Seitenkette, zusätzliche Carboxylgruppe, terminale Methylaminogruppe). Ein Acetylglucosaminrest fehlt bei Dalbavancin, ein Chloratom ist an anderer Stelle positioniert.
Antibakterielle Wirkung, Resistenz
Dalbavancin hemmt – wie andere Glykopeptide – die Zellwandsynthese grampositiver Bakterien. Die Heptapeptid-Grundstruktur des Moleküls bindet an die C-terminale Peptidstruktur D-Ala-D-Ala der Peptidoglykan-Vorstufen (Lipid II) der Zellwandsynthese. Durch die Komplexbildung werden die Polymerisation und Quervernetzung der Peptidoglykanstränge blockiert.
Dalbavancin wirkt bakterizid. Es weist eine hohe antibakterielle Aktivität gegen S. aureus und Koagulase-negative Staphylokokken auf. Der MHK90-Wert liegt bei 0,06 mg/l. Auch Vancomycin- (Glykopeptid-) intermediäre Stämme werden erfasst (VISA). Methicillin-Resistenz hat keinen Einfluss auf die Wirksamkeit von Dalbavancin. VanA-resistente Staphylokokken und Enterokokken sind auch gegen Dalbavancin resistent. Gegen Vancomycin-empfindliche Enterokokken ist es potenter als Vancomycin und etwa ebenso aktiv wie Teicoplanin. Auch S. pneumoniae und andere Streptokokken werden bereits bei niedrigen Konzentrationen gehemmt. Im gramnegativen Bereich ist es ebenso wie andere Glykopeptide unwirksam. Von EUCAST wurden folgende Grenzwerte definiert: sensibel ≤ 0,125 mg/l; resistent > 0,125 mg/l.4,5
Pharmakokinetische Eigenschaften
Dalbavancin wird über 30 Minuten als intravenöse Kurzinfusion verabreicht. Aufgrund der langsamen Elimination ist eine Infusion einmal pro Woche ausreichend. Zu Beginn der Therapie werden 1000 mg infundiert, nach einer Woche eine zweite Dosis in Höhe von 500 mg. Nach Anwendung einer Einzeldosis von 1000 mg Dalbavancin bei gesunden Probanden wurden durchschnittlich 19 % bis 33 % der Dosis als Dalbavancin und 8 % bis 12 % als Hydroxy-Dalbavancin im Urin ausgeschieden. Etwa 20 % der verabreichten Dosis werden mit den Fäzes eliminiert.4
Die wichtigsten pharmakokinetischen Parameter können der Tabelle entnommen werden.
Tabelle 1.
Dosierung und pharmakokinetische Parameter von Dalbavancin
|
Dosis |
Tag 1: 1 x 1000 mg i.v. Tag 8: 1 x 500 mg i.v. |
|
Cmax |
Tag 1: 278 ± 53 mg/l Tag 8: 166 ± 43 mg/l |
|
t½ |
Mittelwert: Bereich: |
|
AUC |
10.577 mg/l x h |
|
Proteinbindung
|
93% |
|
VD (steady state) |
15,7 l |
|
Elimination |
Urin, teilweise in metabolisierter Form, und mit den Fäces
|
* nach SPC XYDALBA4
Bei Patienten mit leichter (CLCR 50 - 79 ml/min), mittelschwerer (CLCR 30 – 49 ml/min) und schwerer (CLCR < 30 ml/min) Nierenfunktionsstörung war die mittlere Plasma-Clearance (CLT) um 11%, 35% bzw. 47% im Vergleich zu Probanden mit normaler Nierenfunktion verringert. Bei Patienten mit chronischer Nierenfunktionsstörung, deren Kreatinin-Clearance geringer als 30 ml/min ist und die keine regelmäßige Hämodialyse erhalten, sollte die empfohlene einmal wöchentliche Dosierung für Dalbavancin auf 750 mg reduziert werden, gefolgt von einer zweiten Dosis eine Woche später von 375 mg.4
Die Pharmakokinetik von Dalbavancin bei Patienten mit einer Nierenerkrankung im Endstadium, die eine Dialyse dreimal pro Woche erhielten, war ähnlich wie bei den Patienten mit leichter bis mittelschwerer Nierenfunktionsstörung. Weniger als 6 % der angewendeten Dosis werden nach einer dreistündigen Hämodialyse beseitigt.4
Klinische Studien
In einer Doppelblindstudie wurden 854 Patienten mit komplizierten Haut- und Weichgewebeinfektionen entweder mit zwei Dosen Dalbavancin oder mit Linezolid (ZYVOXID) in üblicher Dosierung von zweimal täglich 600 mg über 14 Tage behandelt. Der Behandlungserfolg und die Verträglichkeit waren in beiden Gruppen gleich gut. Etwa 90% der Patienten zeigten ein positives Therapieresultat.6
In zwei weiteren Studien mit identischem Design (Discover 1 und 2) wurde Dalbavancin mit der Standardtherapie bei Patienten mit Haut- und Weichgewebeinfektionen verglichen. Dabei wurde Vancomycin mindestens drei Tage lang intravenös gegeben, danach bestand die Option der Umstellung auf eine orale Linezolid-Behandlung. Die beiden Studien an insgesamt mehr als 1300 Patienten wurden in den Jahren 2011 und 2012 durchgeführt. Auch hier zeigte sich ein identisches, positives Therapieergebnis von >90% der Behandelten in beiden Gruppen.7
Die Datenlage zur Wirksamkeit von Dalbavancin bei anderen Indikationen ist vergleichsweise eingeschränkt. An einer kleinen Gruppe von 75 Patienten mit einer Katheter-assoziierten Sepsis durch Staphylokokken wurde es mit Vancomycin verglichen. Die Therapie war in 50% (Vancomycin) bzw. 87% (Dalbavancin) der Patienten erfolgreich. Größere zulassungsrelevante Studien liegen für derartige Infektionen nicht vor.8
Verträglichkeit, Interaktionen
In den klinischen Studien der Phasen 2 und 3 erhielten 1.778 Patienten Dalbavancin. Die häufigsten Nebenwirkungen, die bei ≥ 1 % der mit Dalbavancin behandelten Patienten auftraten, waren Übelkeit (2,8 %), Diarrhö (2,5 %), Kopfschmerz (1,5 %), erhöhte Gamma-Glutamyltransferase (1,1 %), Hautausschlag (1,0 %) sowie Erbrechen (1,0 %) und waren in der Regel leicht oder mittelschwer.4
Es wurden keine Studien zur Erfassung von Wechselwirkungen durchgeführt. Dalbavancin wird in vitro nicht durch CYP-Enzyme metabolisiert; es ist nicht bekannt, ob der Arzneistoff ein Substrat für die Leberaufnahme und für Efflux-Transporter ist.
Das Antibiotikum wird während der Schwangerschaft nicht empfohlen. Es gab zwar keine Hinweise auf Teratogenität in den tierexperimentellen Studien, jedoch zeigten Ratten bei Konzentrationen (AUC), die etwa um das dreifache über der klinischen Exposition lagen, verminderte Fruchtbarkeit und ein erhöhtes Auftreten von Embryo-Letalität, ein reduziertes Fetalgewicht und andere reproduktionstoxische Wirkungen.
ZUSAMMENFASSUNG: Dalbavancin (XYDALBA) ist ein Glykopeptid-Antibiotikum, das bei Haut- und Weichgewebeinfektionen zugelassen ist. Es wirkt bakterizid gegen grampositive Bakterien. Im Vergleich zu Vancomycin (diverse Generika) ist die antibakterielle Aktivität erhöht. Nach intravenöser Infusion wird es nur sehr langsam mit einer Halbwertzeit von ca. 16 Tagen eliminiert, es wird daher nur einmal pro Woche verabreicht. In umfangreichen vergleichenden klinischen Studien war es etwa gleich wirksam wie Vancomycin oder Linezolid (ZYVOXID). Die Verträglichkeit war in den Zulassungsstudien gut. Über selten auftretende unerwünschte Wirkungen lässt sich derzeit aber keine abschließende Aussage machen.
Literatur
Ergänzung (2019)
Leitlinie zur Therapie mit parenteralen Antibiotika
Auf die ausführliche PEG S2k Leitlinie (AWMF-Registernummer 082-006) der Paul-Ehrlich-Gesellschaft für Chemotherapie e.v. (PEG) Kalkulierte parenterale Initialtherapie bakterieller Erkrankungen bei Erwachsenen – update 2018 (2. aktualisierte Version; 25. Juli 2019) sei an dieser Stelle hingewiesen.