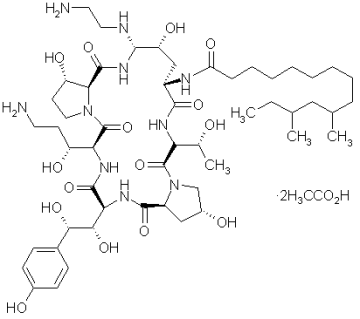
Caspofungin - ein neues Antimykotikum zur Behandlung von Aspergillus-Infektionen
Aktuelle Ergänzungen am Ende des Textes
Die Häufigkeit von Systemmykosen durch Aspergillus und Candida hat in den vergangenen Jahrzehnten kontinuierlich zugenommen. Hintergrund dieser Entwicklung
ist vor allem die steigende Zahl immunsupprimierter Patienten. Nach wie vor ist das Angebot an wirksamen Antimykotika bei diesen schweren, lebensbedrohlichen Infektionen dürftig und beschränkt sich
auf Amphotericin B (AMPHOTERICIN B) und
Azolantimykotika. Daher ist es zu begrüßen, dass mit Caspofungin (CANCIDAS) ein neues Arzneimittel zur Behandlung systemischer Mykosen von der europäischen Arzneimittelbehörde EMEA zugelassen worden
ist. Caspofungin ist der erste Vertreter einer neuen Wirkstoffklasse, der Echinocandine. Das Antimykotikum hemmt die Synthese von ß-(1,3)-D-Glucan, einem essentiellen Bestandteil der Zellwand von
Pilzzellen.
Antimykotische Aktivität
Caspofungin weist in vitro ein breites antimykotisches Spektrum auf. Es wirkt gegen verschiedene Aspergillus- und Candida-Spezies, wobei auch Azol-resistente und Amphotericin-resistente Aspergillus-Stämme erfasst werden. Die in vitro vorhandene antimykotische Aktivität wurde in Tierexperimenten bestätigt. Allerdings bestand keine Wirksamkeit gegen C. neoformans bei immundefizienten Mäusen.
Pharmakokinetische Eigenschaften
Caspofungin wird intravenös verabreicht und ist zu etwa 96% an Plasmaproteine gebunden. Mit einer Halbwertzeit von 9 bis 10 Stunden (ß-Phase) wird die Substanz überwiegend hepatisch eliminiert, ein geringer Teil wird langsamer ausgeschieden (HWZ: 40 bis 50 Stunden). Neben der N-Acetylierung spielen auch hydrolytische Vorgänge eine Rolle. Eine Anpassung der Dosierung bei renaler Insuffizienz scheint nicht notwendig zu sein, bei mittelschwerer Leberinsuffizienz (Child-Pugh Score: 7 – 9) soll die Erhaltungsdosis auf 35 mg / Tag reduziert werden.
Klinische Wirksamkeit
Die klinischen Erfahrungen mit Caspofungin sind bisher noch sehr begrenzt. In den USA steht das Präparat unter dem Handelsnamen CANCIDAS schon seit einigen Monaten zur Behandlung therapierefraktärer Aspergillus-Infektionen zur Verfügung. Die Entscheidung der dortigen Zulassungs-behörde FDA gründete sich auf die ermutigenden Therapieergebnisse bei 63 Patienten mit invasiver Aspergillose, bei denen die Standardtherapie [Amphoterin B oder Itraconazol (SEMPERA u.a.)] ohne Erfolg blieb oder die die Standardtherapie nicht vertrugen. Bei etwa jedem zweiten Patienten wurde ein günstiges Ansprechen auf die alternative Therapie mit Caspofungin festgestellt.
Die Dosierung beträgt initial 70 mg, danach werden 50 mg/Tag verabreicht.
Unerwünschte Wirkungen, Interaktionen
Auch die Fragen zur Verträglichkeit und Sicherheit lassen sich bei diesem Arzneimittel bisher nur unzureichend beantworten, da erst Erfahrungen mit etwa 600 Patienten vorliegen. Am häufigsten waren Fieber, entzündliche Reaktionen an der Infusionsstelle, Übelkeit, Erbrechen oder Kopfschmerzen. Bei etwa jedem 10. Patienten kam es zum Anstieg der Transaminasen. Bei gleichzeitiger Gabe von Ciclosporin (SANDIMMUN) waren die AUC-Werte von Caspofungin um ein Drittel erhöht, die Kinetik von Ciclosporin blieb unbeeinflusst. Ob es weitere klinisch relevante Interaktionen mit anderen hepatisch metabolisierten Arzneistoffen gibt, ist derzeit noch nicht geklärt.
ZUSAMMENFASSUNG
Caspofungin (CANCIDAS) ist ein Antimykotikum mit neuartigem Wirkmechanismus zur intravenösen Verabreichung. Es besitzt in vitro ein breites Spektrum, die klinischen Erfahrungen sind aber noch sehr begrenzt. Daher sollte es zunächst nur restriktiv zur Behandlung von Aspergillus-Infektionen bei Versagen der Standardtherapie angewandt werden.