Aztreonam - welche Bedeutung haben Monobactame?
Aktuelle Ergänzungen am Ende des Textes
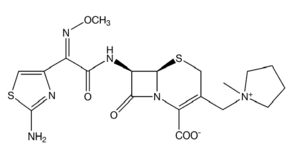
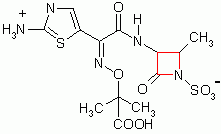
Aztreonam (AZACTAM) - das erste therapeutisch verwendbare "Monobactam" - ist in der Bundesrepublik Deutschland ab April 1985 im Handel. Die Grundstruktur
des Antibiotikums entspricht praktisch einem isolierten ß-Laktamring. Einige Kenntnisse aus den Struktur-Wirkungsbeziehungen bei Cephalosporinen haben die Entwicklung dieser vollsynthetischen
Substanz geprägt. Die Formel beinhaltet einen Aminothiazol-Rest in der Seitenkette, der auch bei einer Reihe von Cephalosporinen die hohe Aktivität im gramnegativen Bereich mitbedingt
[Cefotaxim (CLAFORAN), Cefmenoxim (TACEF), Ceftizoxim (CEFTIX), Ceftriaxon (ROCEPHIN) und Ceftazidim (FORTUM)]. Die größten strukturellen Parallelen
bestehen mit dem zuletzt genannten Präparat.
Mikrobiologie
Enterobakterien und andere aerobe, gramnegative Erreger sprechen gut auf
Aztreonam an. Die MHK90-Werte - also die Konzentrationen, bei denen mindestens 90% der untersuchten Stämme gehemmt werden - liegen z.B. für E. coli, P. mirabilis, H. influenzae und N. gonorrhoeae
deutlich unter 1 mg/l. Eine ähnlich hohe Sensibilität zeigte sich bei der Untersuchung von Klebsiellen und Salmonellen. Insgesamt entspricht dieses Spektrum in etwa dem der oben genannten
Aminothiazol-Cephalosporine. Geringfügig überlegen ist Aztreonam bei manchen indolpositiven Proteus-Stämmen. Für den klinischen Einsatz ist seine Pseudomonas-Aktivität von Interesse: die MHK90-Werte
liegen bei 12 bis 25 mg/l.
Damit ist Aztreonam aktiver als Cefotaxim oder Latamoxef (MOXALACTAM), jedoch deutlich weniger wirksam als Ceftazidim gegenüber diesem "Problemkeim".
Die antibakterielle Wirkung wird bei zahlreichen Erregerstämmen durch Kombination mit Aminoglykosiden - wie z.B. Tobramycin (GERNEBCIN) - erhöht. Es bestand jedoch kein relevanter synergistischer
Effekt zwischen Aztreonam und Penicillinen wie z.B. Azlocillin (SECUROPEN) oder Piperacillin (PIPRIL) gegenüber P. aeruginosa.
Das neue Monobactam besitzt wie die Cephalosporine eine charakteristische "Enterokokken-Lücke". Es ist im gesamten grampositiven Bereich unwirksam (Staphylokokken, Pneumokokken) und beeinflußt
ebensowenig Anaerobier in ihrem Wachstum.[1]
Pharmakokinetik
Aztreonam wird ausschließlich parenteral verabreicht. Nach einer
dreiminütigen intravenösen Injektion von 500, 1000 oder 2000 mg wurden bei gesunden Probanden Serumspiegel von etwa 60, 120 oder 240 mg/l gemessen. Acht Stunden nach der mittleren Dosis liegen die
Spiegel noch bei etwa 3 mg/l.[2] Die Plasmaeiweißbindung wird mit 56% angegeben. Die Eliminationshalbwertzeit liegt zwischen 90 und 120 Minuten. Das Verteilungsvolumen von 0,21 l/kg entspricht in
etwa dem Extrazellulärraum.
Bei normaler Nierenfunktion wird der größte Teil des Antibiotikums (etwa 60 bis 70%) unverändert im Urin ausgeschieden. Insgesamt werden etwa 20% metabolisiert, davon liegt die Hälfte als
Hydrolyseprodukt mit geöffnetem ß-Laktamring vor. [3,4] Dieses Abbauprodukt wird nur sehr langsam ausgeschieden (HWZ: ca. 26 Std.).
Die Halbwertzeit der Ausgangssubstanz (Aztreonam) verlängert sich bei Patienten mit terminaler Niereninsuffizienz auf etwa sechs Stunden. Die totale Clearance zeigt eine enge Korrelation zur
Kreatinin-Clearance und reicht von 107 ml/min (normal) bis zu 29 ml/min bei völligem Funktionsverlust. Wenn die normalen Dosierungsintervalle eingehalten werden, sollte die Dosis des Präparates etwa
bei einer Kreatinin-Clearance von 30 ml/min halbiert werden, oder die Dosierungsintervalle müssen entsprechend verlängert werden.[5]
Klinik
Die üblichen Dosierungsschemata für Aztreonam lauten 3-mal täglich 1,0 bis 4-mal täglich 2,0 g. Das Präparat ist am ehesten zur gezielten Behandlung von nosokomialen Infektionen mit sensiblen gramnegativen Erregern angezeigt. Da es aufgrund seiner antibakteriellen und pharmakokinetischen Eigenschaften besonders bei komplizierten Harnwegsinfektionen in Betracht kommt, wurde es bei dieser Indikation z.B. mit Gentamicin (REFOBACIN u.a.) verglichen.[6]
Es wurden die folgenden, typischen Ergebnisse erzielt:
- Wenn Rezidive und Reinfektionen bei der Bewertung nach 4-6 Wochen mitberücksichtigt werden, war das Behandlungsergebnis mit beiden Antibiotika gleich.
- Das Ergebnis wurde entscheidend durch anatomische Anomalien im Urogenitaltrakt bestimmt - nicht durch die Wahl des Antibiotikums!
- Enterokokken wurden sehr viel häufiger während und nach der Behandlung bei Patienten mit Aztreonam isoliert. Hier zeigte sich ganz klar, daß die Wirkungsschwäche des Monobactams gegenüber Enterokokken durchaus klinische Relevanz besitzt. Man wird auf solche Selektionen und Superinfektionen bei einer Therapie mit Aztreonam achten müssen - ebenso wie beim Einsatz von Cephalosporinen.
- Toxikologisch ist das ß-Laktam-Antibiotikum günstiger zu beurteilen als Gentamicin. Unter der Therapie mit dem Aminoglykosid kam es gelegentlich zum Anstieg des Serum-Kreatinin-Wertes, wobei allerdings die Kausalitätsfrage nicht immer eindeutig zu beantworten war.
- Angesichts dieser Ergebnisse ergeben sich einige Fragen:
- Brauchen wir überhaupt Monobactame? Gibt es eine Lücke in unserer chemotherapeutischen Palette, in die das neue Medikament hineinpaßt? Welchen Stellenwert besitzen die einzelnen Vor- und Nachteile der Substanz? Es wir eine Frage der Zeit, des Marketings und auch des Preises sein, um adäquate Anworten geben zu können!
ZUSAMMENFASSUNG
Aztreonam (AZACTAM) ist das erste verfügbare "Monoactam". Das Molekül
zeigt zwar eine neuartige Grundstruktur, aber die Substituenten sind ähnlich wie bei den neueren Cephalosporinen. Es besitzt eine hohe Aktivität gegen zahlreiche gramnegative Erreger. Die Wirkung auf
P. aeruginosa ist geringer als die der aktivsten Cephalosporine. Im grampositiven Bereich und gegen Anaerobier ist es unwirksam. Nach parenteraler Gabe wird es mit einer Halbwertzeit von 1,5 bis 2
Stunden überwiegend unverändert renal eliminiert. Aztreonam stellt ein weiteres Alternativpräparat zur gezielten Behandlung nosokomialer Infektionen durch gramnegative Erreger
dar.
1 SYKES, R.B. et al.
Antimicrob. Agents Chemother. 21: 85-92, 1982
Antimicrob. Agents Chemother. 21: 944-949, 1982
Antimicrob. Agents Chemother. 24: 394-400, 1983
Antimicrob. Agents Chemother. 23: 125-132, 1983
Antimicrob. Agents Chemother. 24: 252-261, 1983
Lancet 1: 1315-1318, 1984
Ergänzungen (November 2000)
Aztreonam ist nach wie vor das einzige Monobactam, das zur antibakteriellen Therapie zur Verfügung steht.
Seit der Erstellung und Veröffentlichung dieses Artikels in der Zeitschrift für Chemotherapie (Heft 2, 1985) sind zahlreiche weitere Arbeiten über Aztreonam publiziert worden. Insbesondere soll an
dieser Stelle auf die folgenden Publikationen hingewiesen werden:
Brogden RN, Heel RC. Aztreonam. A review of its antibacterial activity, pharmacokinetic
properties and therapeutic use. Drugs. 1986;31:96-130
Koch C, Hjelt K, Pedersen SS, Jensen ET, Jensen T, Lanng S, Valerius NH,
Pedersen M, Hoiby N. Retrospective clinical study of hypersensitivity reactions to aztreonam and six other beta-lactam antibiotics in cystic fibrosis patients receiving multiple treatment
courses.
Rev Infect Dis. 1991;13 (Suppl 7):S608-S611.
Ergänzungen (2010)
Mit Aztreonam-Lysin (CAYSTON) steht eine neu entwickelte Zubereitungsform des Monobactamantibiotikums zur Inhalation zur Verfügung, das bei Patienten mit Mukoviszidose angewandt werden kann.