Avibactam – ein neuer ß-Laktamase-Inhibitor in Kombination mit Ceftazidim
Unveränderter Text aus Heft 4, 2016
Ergänzungen am Ende des Textes
Die Bildung von ß-Laktamasen ist eine der wichtigsten Abwehrreaktionen eines Bakteriums, um sich vor einem Antibiotikum zu schützen. Eine enorme Vielfalt möglicher Enzyme ist bekannt, die den Erregern Resistenz gegen ß-Laktamantibiotika verleihen. Bereits seit den frühen 1980er Jahren wird die Clavulansäure mit Amoxicillin kombiniert (AUGMENTAN u.a.), um durch Hemmung der ß-Laktamasen das Antibiotikum vor der Inaktivierung zu schützen. Zwei weitere ß-Laktamase-Inhibitoren, Sulbactam (COMBACTAM u.a.) und Tazobactam (in: TAZOBAC u.a.), sind ebenfalls seit langem verfügbar und werden in verschiedenen Kombinationen mit Penicillinen angewandt. Das erste Kombinationspräparat aus einem Cephalosporin und einem ß-Laktamase-Inhibitor wurde unter dem Namen ZERBAXA (Ceftolozan plus Tazobactam) vor etwa einem Jahr zugelassen.
Neu verfügbar ist nun die Kombination aus 500 mg Avibactam und 2000 mg Ceftazidim (FORTUM u.a.), das in Europa unter dem Handelsnamen ZAVICEFTA zugelassen und in den USA als AVYCAZ erhältlich ist. Während die drei bisher bekannten ß-Laktamase-Inhibitoren eine ß-Laktamgrundstruktur besitzen, gehört Avibactam zu den Diazabicyclooctanen, einer Gruppe von synthetischen Verbindungen, deren Eigenschaften bereits in den 1990er Jahren in den Laboratorien von Hoechst Marion Roussel (HMR) untersucht wurden.1
Mit ZAVICEFTA kommt also ein zweites Kombinationspräparat aus einem Cephalosporin und einem ß-Laktamase-Inhibitor in den Handel. Eine Entwicklung, die bei Einführung des Ceftazidim (FORTUM u.a.) Mitte der 1980er Jahre nicht erwartet wurde. Damals galt die ß-Laktamase-Stabilität dieses halbsynthetischen Cephalosporins als ausgezeichnet; heute muss man feststellen, dass die Bakterien sich durch neue ß-Laktamasen zunehmend der Wirkung der Antibiotika entziehen. ß-Laktamase-Inhibitoren tragen dazu bei, den Vorsprung – zumindest teilweise - wieder aufzuholen.
Inhibition der ß-Laktamasen, antibakterielles Spektrum
In vitro hemmt Avibactam die ß-Laktamasen der Ambler-Klasse A, wie zum Beispiel die KPC- und ESBL-Enzyme. Eine Inhibition ist auch bei Enzymen der Klasse C und bei einigen Klasse D-Enzymen zu beobachten (Tabelle 1). Vergleicht man die Hemmwirkung der verschiedenen ß-Laktamase-Inhibitoren gegen das Enzym AmpC, so ergibt sich eine halbmaximale Inhibition bei den folgenden Konzentrationen: > 100 µM (Clavulansäure), 4,6 µM (Tazobactam) und 0,1 µM (Avibactam).2
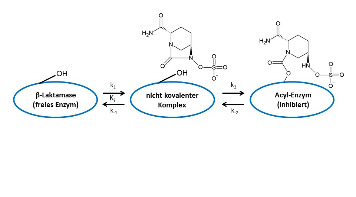
Die Abbildung zeigt die kovalente Bindung von Avibactam an die ß-Laktamase TEM-1. Im Gegensatz zu den drei anderen, bisher angewandten Inhibitoren mit ß-Laktamgrundstruktur ist die Acylierung des bakteriellen Enzyms reversibel. Die Ablösung des Inhibitors von dem Enzym erfolgt unter Regeneration des Inhibitormoleküls. Für diesen Vorgang wurde eine Halbwertzeit von 16 Minuten gemessen.3
ß-Laktamasen der Klasse B, die Metallo-ß-Laktamasen, werden nicht gehemmt.4 Wenn die Erreger derartige ß-Laktamasen produzieren, sind sie resistent gegen Ceftazidim / Avibactam. Weitere Möglichkeiten der Resistenz bestehen in der Ausbildung von Efflux-Mechanismen und durch Veränderung der Penicillin-bindenden Proteine, also des molekularen Angriffspunktes der ß-Laktamantibiotika.
Abbildung: Reversible Bindung von Avibactam an ein Molekül der ß-Laktamase TEM-1. Bei der Ablösung des Inhibitors wird der fünfgliedrige Harnstoffring wieder geschlossen. Damit besteht ein grundsätzlicher Unterschied zu den Hemmstoffen mit ß-Laktamstruktur, denn der viergliedrige ß-Laktamring kann nicht wieder geschlossen werden.3
Tabelle 1:
Hemmung von ß-Laktamasen durch Tazobactam und Avibactam4
|
Klasse |
ß-Laktamase |
Substrate |
Hemmung durch: Taz / Avi
|
|
A |
TEM-1, TEM-2, SHV-1 |
Penicilline, ältere Cephalo-sporine |
++ / ++ |
|
A |
TEM-3, SHV-2, CTX-M-14 |
Cephalo-sporine mit erweitertem Spektrum, Monobactame |
++ / ++ |
|
A |
KPC-2, KPC-3 |
ß-Laktame, einschl. Carbapeneme |
0 / ++ |
|
B |
IMP-1, NDM-1, VIM-1 |
ß-Laktame, einschl. Carbapeneme (nicht: Monobactame) |
0 / 0 |
|
C |
AmpC aus Escherichia coli |
Cephalo-sporine |
+ / ++
|
|
D |
OXA-48 |
Carbapeneme |
0 / ++
|
++ = Hemmung;
+ = Hemmung bei hohen Konzentrationen;
O = keine Hemmung
Die Kombination ist aktiv gegen gramnegative Erreger wie Enterobacteriaceae oder P. aeruginosa, die Grenzkonzentration zur Unterscheidung zwischen empfindlichen und resistenten Erregern liegt bei ≤ 8 (4) mg/l. Das Ausmaß der Aktivitätssteigerungen soll an zwei Beispielen dargestellt werden: bei Carbapenemase-produzierenden Klebsiella pneumoniae (OXA-48), sinken die Hemmkonzentrationen von 512 auf 0,5 mg/l, bei ESBL-positiven E. coli-Stämmen von 32 auf 0,25 mg/l.2
Von besonderem Interesse ist die Aktivität gegen P. aeruginosa. Bei diesem Erreger sind 32 mg Ceftazidim/l Medium notwendig, um mindestens 90% der Stämme zu hemmen, bei Zusatz von Avibactam reduziert sich die MHK90 auf 8 mg/l. Auch bei einer Gruppe von 38 Stämmen mit Resistenz gegen Meropenem (MERONEM u.a.) lagen die MHK90-Werte für Ceftazidim / Avibactam bei 8 mg/l, während für Meropenem eine Konzentration von 32 mg/l ermittelt wurde. Die Untersuchung fand im direkten Vergleich mit der Kombination aus Ceftolozan / Tazobactam statt, für die eine MHK90 von 4 mg/l bestimmt werden konnte. Bei beiden Kombinationen lag die Resistenzrate bei 8%.5
Die Aktivität von Ceftazidim mit oder ohne Inhibitor gegen grampositive und anaerobe Erreger ist gering. Wegen der schwachen Aktivität gegen Bacteroides fragilis wurde in den klinischen Studien bei Patienten mit intraabdominellen Infektionen gleichzeitig Metronidazol (diverse Handelsnamen) gegeben.
Pharmakokinetische Eigenschaften
Avibactam weist ein sehr ähnliches pharmakokinetisches Verhalten auf wie Ceftazidim. Bei gesunden, erwachsenen Männern wurden die in der Tabelle zusammengestellten Daten ermittelt. Die Teilnehmer hatten elf Tage lang jeweils drei Infusionen der Kombination in üblicher therapeutischer Dosierung der beiden Inhaltsstoffe erhalten. Die beiden Wirkstoffe werden zu weniger als 10% an Proteine gebunden und ganz überwiegend unverändert renal ausgeschieden. Bei gering eingeschränkter Nierenfunktion (CLCR: 31 bis 50 ml/min) wird die Dosis halbiert, bei einer Kreatinin-Clearance unter 30 ml/min wird bei halber Dosis das Dosisintervall verlängert.
Tabelle 2:
Pharmakokinetische Daten von Ceftazidim und Avibactam nach mehrfacher Gabe*
|
|
Ceftazidim |
Avibactam
|
|
Dosis (mg) |
2000 |
500
|
|
Cmax (mg/l) |
90 |
15
|
|
AUC (mg x h /l) |
291 |
38
|
|
t½ (h) |
2,7 |
2,7
|
|
Cl (l/h) |
6,9 |
13
|
|
Vss (l) |
17 |
22
|
* 11 Tage lang, dreimal täglich als 2-stündige Infusion
(nach: Full Prescribing Information AVYCAZ), Werte gerundet
Klinische Studien
Das Kombinationspräparat ist laut Empfehlung des zuständigen Komitees (CHMP) der Europäischen Zulassungsbehörde (EMA) für die Behandlung der folgenden Infektionen bei Erwachsenen indiziert:
- Komplizierte abdominelle Infektionen,
- Komplizierte Harnwegsinfektionen,
- nosokomial erworbene Pneumonien (HAP),
einschließlich Pneumonien bei beatmeten Patienten (VAP).
Damit besteht ein bemerkenswerter Unterschied zu der Situation in den USA, wo das Präparat bei nosokomialen Pneumonien derzeit nicht zugelassen ist.
In den klinischen Studien erwies sich die Kombination aus Ceftazidim / Avibactam als gut wirksam und verträglich.6 Das Nebenwirkungsprofil entsprach dem des Ceftazidims. Die umfangreichsten Erfahrungen liegen bisher bei Patienten mit komplizierten abdominellen Infektionen vor. Bei Patienten mit Infektionen des Bauchraums zeigte sich das Cephalosporin mit Inaktivierungssschutz im Vergleich zu Meropenem als nicht unterlegen. Nach Behandlung mit Ceftazidim / Avibactam plus Metronidazol wurde bei 83% der Patienten (mITT – modified intention-to-treat) eine Heilung nach klinischen Kriterien festgestellt, 85% waren es in der Meropenem-Gruppe. Bei Patienten mit eingeschränkter Nierenfunktion (ClCR 30 bis 50 ml/min) war der Therapieerfolg geringer (45% vs. 74%), was durch eine zu niedrige Dosierung erklärt werden könnte. In den Studien wurde bei niereninsuffizienten Patienten die halbe Normdosis zweimal täglich gegeben, aktuell werden jedoch drei Infusionen pro Tag empfohlen. Zu den häufigsten unerwünschten Wirkungen zählten in beiden Gruppen gastrointestinale Beschwerden; Übelkeit (10% vs. 6%) und Erbrechen (14% vs. 5%) waren in der Meropenem-Gruppe seltener als nach Behandlung mit der Kombination. Zum Teil war die schlechtere Verträglichkeit der Kombinationstherapie offenbar auf die Gabe von Metronidazol zurückzuführen.4 Die Verträglichkeit war deutlich besser in einer Studie bei Patienten mit komplizierten Harnwegsinfektionen, in der das Antibiotikum deutlich niedriger dosiert wurde (3 x tgl. 500 / 125 mg Ceftazidim / Avibactam). Als Vergleichspräparat diente Imipenem / Cilastatin (ZIENAM u.a.). In dieser Studie an einer relativ geringen Zahl von Patienten kam es in keinem Fall zum Erbrechen eines Patienten.7
ZUSAMMENFASSUNG:
Avibactam ist ein neu entwickelter ß-Laktamase-Inhibitor der in Kombination mit Ceftazidim (FORTUM u.a.) unter dem Namen ZAVICEFTA in den Handel kommt. Avibactam hemmt die meisten ß-Laktamasen, jedoch nicht die Enzyme der Gruppe B, die Metallo-ß-Laktamasen. Bei zahlreichen gramnegativen Erregern kann die Resistenz gegen Ceftazidim durch Zusatz von Avibactam überwunden werden. Das Kombinationspräparat ist bei komplizierten Harnwegsinfektionen und bei nosokomialen Pneumonien zugelassen. Bei intraabdominellen Infektionen wird es in Kombination mit Metronidazol (diverse Handelsnamen) gegeben. Die Verträglichkeit ist gut, sie entspricht der Verträglichkeit von Ceftazidim.
Literatur:
1. Coleman K. Diazabicyclooctanes (DBOs): a potent new class of non-β-lactam β-lactamase inhibitors. Curr Opin Microbiol. 2011 Oct;14(5):550-5
2. Zhanel GG et al. Ceftazidime-avibactam: a novel cephalosporin/β-lactamase inhibitor combination. Drugs. 2013 Feb;73(2):159-77
4. van Duin D, Bonomo RA. Ceftazidime/Avibactam and Ceftolozane/Tazobactam: Second-generation β-Lactam/ β-Lactamase Combinations. Clin Infect Dis. 2016;63:234-241
7. Full Prescribing Information AVYCAZ, September 2015, rev. June 2016
Ergänzung (August 2016)
Zusammenfassung der Merkmale des Arzneimittels und andere Informationen der EMA zu ZAVICEFTA
Ergänzung (2019)
Leitlinie zur Therapie mit parenteralen Antibiotika
Auf die ausführliche PEG S2k Leitlinie (AWMF-Registernummer 082-006) der Paul-Ehrlich-Gesellschaft für Chemotherapie e.v. (PEG) Kalkulierte parenterale Initialtherapie bakterieller Erkrankungen bei Erwachsenen – update 2018 (2. aktualisierte Version; 25. Juli 2019) sei an dieser Stelle hingewiesen.