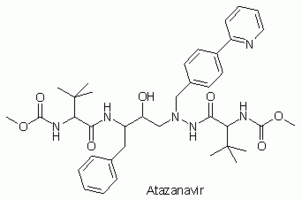
Atazanavir
ein neuer Protease-Inhibitor zur einmal täglichen Gabe
Aktuelle Ergänzungen am Ende des Textes
Das HI-Virus benötigt für seine Ausbreitung eine Reihe von Proteinen, die bei der Vermehrung zunächst in Form von Vorläufer-Proteinen synthetisiert werden.
Die anschließende Zerschneidung dieser Vorläufer-Proteine erfolgt durch eine spezifisch wirksame virale Protease, welche die Peptidbindung zwischen zwei Aminosäuren spalten kann. Aufgrund der hohen
Spezifität der Protease bietet das aktive Zentrum dieses Enzyms einen geeigneten Angriffspunkt für antiretrovirale Wirkstoffe. Durch die Herstellung von Substanzen, die Peptid-ähnliche Strukturen
aufweisen, ist es bekanntlich gelungen, Virustatika zu entwickeln, die einerseits eine hohe Affinität zum katalytischen Zentrum der HIV-Protease aufweisen; da sie andererseits jedoch chemisch
modifizierte Peptidbindungen aufweisen, die nicht gespalten werden können, resultiert eine Inhibition der Protease.
Seit 1996 sind insgesamt 6 Protease-Inhibitoren in Deutschland eingeführt worden , durch ihren Einsatz als Bestandteil der antiretroviralen Kombinationstherapie konnte die AIDS-Sterblichkeit
erheblich gesenkt werden. Allerdings besitzen die bisher bekannten Protease-Inhibitoren auch einige Nachteile und optimierte Derivate werden seit Jahren erwartet. Da es sich bei der antiretroviralen
Kombinationstherapie um eine lebenslange Behandlung handelt, sind vor allem Modifikationen erwünscht, die zu einer verbesserten Patienten-Compliance führen können. Bekanntlich erfordert die
antiretrovirale Therapie in hohem Maße die Kooperation des Patienten, denn bereits eine geringe Unregelmäßigkeit bei der Einnahme kann zur Entstehung und Selektion resistenter Virusmutanten führen,
die mit einem Versagen der Therapie einhergehen.
Antivirale Aktivität
Atazanavir (REYATAZ) ist ein neuer Protease-Inhibitor, der erstmals die
einmal tägliche Gabe ermöglicht und dadurch die Kombinationstherapie für den Patienten nicht nur komfortabler sondern auch risikoärmer macht. Da im Molekül eine CH-Gruppe durch ein Stickstoffmolekül
ersetzt wurde, wird die Verbindung auch als Azapeptid bezeichnet. Es hemmt in vitro die HIV-1-Vermehrung bereits bei Konzentrationen im Bereich von 2 – 5 nM (EC50-Werte; 1 nM = 0,7 µg / l).1,2
Resistente Mutanten konnten sowohl in vitro als auch aus dem Blut von Patienten isoliert werden. Dabei handelte es sich in den allermeisten Fällen um den Austausch der von Isoleucin gegen Leucin an
Position 50 (I50L) in der Aminosäuresequenz der Protease; interessanter weise war diese Veränderung mit einer erhöhten Empfindlichkeit der Viren gegen andere Protease-Inhibitoren verbunden.
Andererseits waren Viren mit Resistenz gegen 1 oder 2 andere Protease-Inhibitoren zu mehr als 80% empfindlich gegen Atazanavir. Es besteht also nur eine partielle Kreuzresistenz zu anderen
Protease-Inhibitoren.1,3
Pharmakokinetische Eigenschaften
Innerhalb von etwa 2,5 Stunden nach der Einnahme des Medikamentes in einer Dosierung von 400 mg werden im Plasma Spitzenspiegel erzielt. Bei gleichzeitiger Aufnahme einer leichten Mahlzeit wird die
Bioverfügbarkeit deutlich erhöht und die Variabilität der Spiegel ist geringer, als bei einer Einnahme auf nüchternen Magen. Bei täglicher Einnahme von 400 mg werden „steady-state-Spiegel“ etwa nach
4 bis 8 Tagen erreicht. Im Blut liegen 86% des Wirkstoffs in proteingebundener Form vor; im Liquor konnten nur sehr niedrige Spiegel gemessen werden. Die Metabolisierung erfolgt vor allem in der
Leber durch Cytochrom-P450-abhängige Monooxygenasen; nur etwa 7% werden unverändert im Urin ausgeschieden. In vitro Untersuchungen zeigten, dass der Abbau hauptsächlich über das Isoenzym CYP3A
vermittelt wird. Die Elimination erfolgt mit einer mittleren Halbwertszeit von etwa 7 Stunden. Bei hepatischer Insuffizienz erfolgt die Ausscheidung langsamer; die Halbwertszeit wurde mit 12,1
Stunden im Vergleich zu 6,4 Stunden bei gesunden Probanden errechnet. Es liegen bisher keine Informationen über die Ausscheidung bei Patienten mit Niereninsuffizienz vor.1, 2, 4
Klinische Studien
Die Wirksamkeit und Verträglichkeit von Atazanavir wurde in drei großen
klinischen Studien bei zuvor unbehandelten Patienten untersucht.1,5 In zwei Studien wurde Nelfinavir zum Vergleich herangezogen, in der dritten Studie war es Efavirenz. In allen Fällen wurde die
Therapie in Kombination mit Nukleosid-Analoga, wie Didanosin, Stavudin, Lamivudin (EPIVIR)
oder Zidovudin (RETROVIR)
durchgeführt. Insgesamt war Atazanavir etwa gleich gut wirksam, wie die Vergleichssubstanzen. In der größten dieser Studien, die an mehr als 800 Patienten durchgeführt wurde, wiesen 67% der
Atazanavir-behandelten Patienten weniger als 400 Kopien der viralen RNA pro Milliliter Blut auf (Efavirenz: 62%). Bei etwa einem Drittel der Patienten lag der Wert sogar unter 50 Kopien / ml Blut
(Atazanavir: 32%; Efavirenz: 37%).
Insbesondere in der Kombination 300mg Atazanavir plus 100mg Ritonavir (NORVIR) über einen Zeitraum von 48 Wochen wurden günstige Resultate erzielt.
Interaktionen
Ähnlich wie alle anderen bekannten Protease-Inhibitoren hemmt Atazanavir vor allem das Cytochrom-Enzym CYP3A4, die Inhibition von anderen Cytochromen, wie CYP1A2 oder CYP2C9 ist schwächer. Darüber hinaus wurde neben der Inhibition von Enzymen des oxidativen Phase-I-Metabolismus auch eine Hemmung der UGT1A1 festgestellt, also eines Phase-II-Enzyms, welches die Übertragung von Glucuronsäure katalysiert. In zahlreichen Studien wurden die möglichen Interaktionen zwischen Atazanavir und anderen gleichzeitig gegebenen Arzneimitteln untersucht. Bei gleichzeitiger Gabe von Efavirenz (SUSTIVA) waren die Konzentrationen von Atazanavir deutlich reduziert, die Spiegel von gleichzeitig gegebenem Clarithromycin (KLACID u.a.) waren etwa verdoppelt, während der wirksame Metabolit des Makrolid-Antibiotikums in deutlich geringeren Konzentrationen im Plasma gemessen wurde (AUC-Werte). Einige Arzneimittel, wie Midazolam (DORMICUM ua.), Ergot-Alkaloide oder das Neuroleptikum Pimozid (ORAP) sind bei Patienten, die mit Atazanavir oder anderen Protease-Inhibitoren behandelt werden, kontraindiziert. Da die Resorption von Atazanavir aus dem Magen-Darmtrakt vom pH-Wert abhängig ist, können gleichzeitig verabreichte Arzneimittel, die zu einer Pufferung der Magensäure führen, eine deutliche Reduktion der Resorption bewirken. Eine Studie mit gleichzeitig gegebenem Stavudin (ZERIT) und Didanosin (VIDEX, gepufferte Tabletten) zeigte, dass die Atazanavir-Spiegel um mehr als 80% reduziert waren. Erfolgte jedoch die Einnahme von Atazanavir 1 Stunde nach den anderen Virustatika, war die Resorption nicht mehr beeinträchtigt. (Detaillierte Tabellen über die Interaktionen mit Atazanavir)
Unerwünschte Wirkungen
Die während der Gabe von Atazanavir beobachteten unerwünschten Wirkungen unterscheiden sich zum Teil deutlich von denen der anderen Protease-Inhibitoren. Die insgesamt gute Verträglichkeit drückt sich darin aus, dass schwerwiegende Nebenwirkungen oder Therapieabbrüche während der klinischen Prüfung nicht häufiger waren als in den Vergleichsgruppen. Übelkeit war die häufigste gastrointestinale Nebenwirkung; Diarrhöen traten deutlich seltener als in den Vergleichsgruppen auf. Eines der größten Probleme bei der langfristigen Therapie mit Protease-Inhibitoren sind die Hyperlipidämie und Lipodystrophie. Unter Atazanavir waren Veränderungen im Fettstoffwechsel im Vergleich mit anderen Protease-Inhibitoren geringer ausgeprägt. So kam es zum Beispiel in einer Vergleichsstudie bei den mit Atazanavir behandelten Patienten nicht zu Fettstoffwechselstörungen, während ein Anstieg der Triglyzeridwerte bei jedem 2. Patienten unter Lopinavir / Ritonavir (KALETRA) registriert wurde. Sehr häufig wurde bei Atazanavir-behandelten Patienten jedoch ein erhöhtes Bilirubin festgestellt. Diese Veränderung war nicht mit einem Anstieg der Transaminasen assoziiert und lässt sich durch die Hemmung der hepatischen Glucuronidierung erklären. Bei etwa 10% der Patienten führte diese Veränderung zum Ikterus, der bei Absetzen des Arzneimittels reversibel war.
ZUSAMMENFASSUNG
Atazanavir (REYATAZ) ist ein neuer Protease-Inhibitor, der in
Kombination mit anderen Virustatika zur antiretroviralen Therapie von HIV-positiven, vorbehandelten Patienten angewandt werden kann. Die zugelassene Dosierung beträgt 300mg Atazanavir plus 100mg
Ritonavir (NORVIR) täglich. Die antivirale Aktivität ist mit dem der anderen Protease-Inhibitoren vergleichbar, es besteht nur teilweise eine Kreuzresistenz. Atazanavir wird langsam eliminiert,
wodurch eine einmal tägliche Gabe ermöglicht wird. Dies ist mit den anderen derzeit verfügbaren Protease-Inhibitoren nicht möglich und stellt einen Fortschritt dar. In klinischen Studien war
Atazanavir gut wirksam und verträglich. Insbesondere sind die relativ geringen Einflüsse auf den Lipidstoffwechsel von Bedeutung. Hinsichtlich des Interaktionspotenzials besteht kein wesentlicher
Unterschied zu anderen Protease-Inhibitoren. Durch Hemmung der Glucuronidierung kommt es sehr häufig zu einem Anstieg des Bilirubins, der mit einem Ikterus assoziiert sein kann, aber nicht als
Symptom einer hepatotoxischen Reaktion gewertet werden darf.
1. ReyatazTM, Full prescribing Information, Bristol Myers Sqibb, 2003
2. BECKER, S.
Expert Rev Anti-infect Ther 2003; 1: 403 - 413
3.
COLONNO RJ, THIRY A et al. Activities of atazanavir (BMS-232632) against a
large panel of human
immunodeficiency virus type 1 clinical isolates resistant to one or more approved protease inhibitors.
Antimicrob Agents Chemother. 2003 Apr;47(4):1324-33.
4.
GOLDSMITH DR, PERRY CM.
Atazanavir.
Drugs. 2003;63(16):1679-93; discussion 1694-5.
5.
SANNE I, PILIERO P et al.
Results of a phase 2 clinical trial at 48 weeks (AI424-007): a dose-ranging, safety, and
efficacy comparative trial of atazanavir at three doses in combination with
didanosine and stavudine in
antiretroviral-naive subjects. J Acquir Immune Defic Syndr. 2003 Jan
1;32(1):18-29.
|
Hinweis: Aktuelle Informationen in englischer Sprache über geeignete Arzneimittel, Behandlungsrichtlinien, aktuelle klinische Studien und andere Aspekte der antiretroviralen Therapie finden Sie unter www.aidsinfo.nih.go |
Aktuelle Ergänzungen (Juli 2009)
Atazanavir muss nur einmal täglich genommen werden. Es war im Vergleich mit Efavirenz (SUSTIVA) klinisch gleich wirksam. Aufgrund der vorliegenden klinischen Studien ist es bisher nur bei antiretroviral vorbehandelten Patienten zugelassen. Derzeit wird Atazanavir/r in einer großen Studie („CASTLE“) im Vergleich zu Lopinavir/r untersucht, um die Zulassung zu erweitern. In der CASTLE-Studie werden in beiden Gruppen Tenofovir (VIREAFD) und Emtricitabin (EMTRIVA) als Kombinationspartner eingesetzt (Kombinationspräparat: TRUVADA). Bis auf Lopinavir, das zweimal täglich gegeben wird, werden die anderen Virustatika in dieser klinischen Studie nur einmal täglich verabreicht.
J Acquir Immune Defic Syndr. 2004 Aug 15;36(5):1011-9.
SWAINSTON HARRISON T, SCOTT LJ. Atazanavir: a review of its use in the management of HIV infection.
Drugs. 2005;65(16):2309-36.
ANSON BD, WEAVER JG et al. Blockade of HERG channels by HIV protease inhibitors.
Lancet. 2005 Feb 19-25;365(9460):682-6.
CHARBIT B, ROSIER A et al. Relationship between HIV protease inhibitors and QTc interval duration in HIV-infected patients: a
cross-sectional study. Br J Clin Pharmacol. 2009 Jan;67(1):76-82