Aciclovir - ein neues Virustatikum
Unveränderter Text aus ZCT Heft 4, 1983
Aktuelle Ergänzungen am Ende des Textes
Virale Infektionen werden in steigendem Maße als Ursache für die Morbidität und Mortalität von Krebspatienten erkannt. Hierbei ist die Herpesvirus-Gruppe (Herpes simplex, Varizella-Zoster, Zytomegalie- und Epstein-Barr-Virus) von besonderer klinischer Bedeutung. Während dem Arzt für die Behandlung bakterieller Erkrankungen eine Vielzahl wirksamer Substanzen zur Verfügung steht, trifft dies auf die Behandlung viraler Erkrankungen nicht zu. Um so erfreulicher ist es, daß in den letzten Jahren mehrere Virustatika in die klinische Prüfung aufgenommen werden konnten, darunter auch Aciclovir (ZOVIRAX). Diese Substanz wurde jetzt vom Bundesgesundheitsamt für die Bundesrepublik Deutschland zugelassen.
Chemie
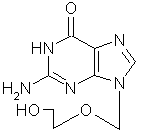
Aciclovir (ZOVIRAX), ein Nucleosid-Derivat mit der chemischen Bezeichnung 9-(2-Hydroxyethoxymethyl)-guanin, wird als parenterale Injektionslösung und als Augensalbe angeboten.
Strukturformal Aciclovir (ein azyklisches Guanosinderivat)
Pharmakodynamik
Die antivirale Wirkung von Aciclovir beschränkt sich auf die Herpes simplex-Viren (HSV) Typ I und II und die Varizella-Zoster-Viren (VZV). Die mittlere Hemmkonzen-tration liegt für HSV Typ I bei 0,15 µmol/l, für Serotyp II bei 1,62 µmol sowie für VZV bei 3,175 µmol/l.
Aciclovir hemmt die Virus-DNA-Synthese durch Blockade der Virus-DNA-Polymerase. Zuvor muß es jedoch erst durch
Virus-spezifische (Thymidin-Kinase) und zelluläre Enzyme phosphoryliert werden. Die zelluläre DNA-Polymerase wird im Gegensatz zur viralen nur geringfügig beeinflußt.
Pharmakokinetik
Der Serumkonzentrationsverlauf von Aciclovir kann am besten mit einem
Zwei-Kompartiment-Modell beschrieben werden. Nach einer intravenösen Gabe von 5 mg/kg KG Aciclovir werden Serummaximal-Konzentrationen erreicht, die deutlich über den minimalen Hemmkonzentrationen
für sensible Viren liegen. Die Substanz wird mit einer Halbwertzeit von 2,9 Stunden vorwiegend renal eliminiert. 50 bis 93% (im Mittel 70,2%) der Dosis werden unverändert im 72-Stunden-Urin
ausgeschieden. Aciclovir wird sowohl glomerulär filtriert als auch tubulär sezerniert, so daß Probenecid (BENEMID) die renale Ausscheidung von Aciclovir um etwa 30% verringert. Wegen der vorwiegend
renalen Ausscheidung kommt es bei eingeschränkter Nierenfunktion zu einem Anstieg der Eliminations-halbwertzeit.
Der Rest der Substanz wird im Organismus vorwiegend zu Hydroxy- und Carboxyderivaten metabolisiert, die virustatisch geringer wirksam sind.
Bei Applikation am Auge werden im Kammerwasser durchschnittlich 7,5 µmol/l Aciclovir erreicht, im Serum sind die Spiegel nicht meßbar.
Klinik
In zahlreichen randomisierten und doppelblind durchgeführten Untersuchungen zeigte sich eine günstige Beeinflussung sowohl des primären als auch rezidivierenden Herpes simplex bei sonst gesunden Patienten hinsichtlich Abheilung, Schmerzreduktion oder Bildung neuer Läsionen, wobei die parenterale Applikation der lokalen überlegen war. Die Rezidiv-neigung wurde nicht beeinflußt. Gleiche Erfahrungen wurden mit der parenteralen Zubereitungsform bei immunsupprimierten Patienten mit Herpes simplex-Infektionen sowohl in der Therapie als auch in der Prophylaxe gewonnen, wenngleich das Latenzstadium nicht verhindert werden konnte. Erste Ergebnisse in der Behandlung von Zoster-Infektionen bei Patienten mit und ohne Immunsuppression sind vielversprechend. Für diese Indikation ist das Präparat jedoch zur Zeit noch nicht zugelassen.
Nebenwirkungen
Im allgemeinen ist Aciclovir gut verträglich. Sehr selten wurden Überempfindlichkeitsreaktionen mit Hautefflores-zenzen beobachtet. Anstieg des Harnstoffes, des Kreatinins sowie der Transaminasen im Serum waren in der Regel reversibel und kurzfristig. Selten wurden zentralnervöse Reaktionen beschrieben.
Resistenz
Drei Resistenzmechanismen wurden beschrieben, wobei die Resistenz durch Fehlen der Thymidinkinase zahlenmäßig überwiegt. Aufgrund der gleichzeitig abgeschwächten Pathogenität dieser resistenten Viren sowie des seltenen Auftretens ist die klinische Bedeutung abschließend noch nicht zu beurteilen.
Dosierung
Zur parenteralen Behandlung viszeraler wie mukokutaner Manifestationen von VZV- wie HSV-Infektionen wird eine Dosierung von
3-mal 5 mg/kg Körpergewicht Aciclovir empfohlen. Bei niereninsuffizienten Patienten muß die Dosierung entsprechend reduziert werden. Die Behandlungsdauer beträgt im Durchschnitt fünf Tage, muß jedoch
dem klinischen Einzelfall angepaßt werden.
ZUSAMMENFASSUNG
Aciclovir (ZOVIRAX) ist ein neues, spezifisch gegen Herpes simplex vom Typ I und II und Varizella-Zoser-Viren wirkendes Virustatikum aus der Klasse der Nukleosid-Derivate. Es liegt für die lokale Anwendung als Salbe und für die parenterale Anwendung als Injektionslösung vor. Nach intravenöser Gabe wird die Substanz mit einer Halbwertzeit von knapp 3 Stunden vorwiegend renal eliminert. Aufgrund dieser Eliminationsmechanismen muß die Dosierung des Aciclovir bei Niereninsuffizienz der aktuellen renalen Funktion angepaßt werden. In verschiedenen randomisierten und prospektiv durchgeführten Untersuchungen zeigte sich eine gute Wirksamkeit des Chemotherapeutikums in der Therapie von mukokutanen und viszeralen HSV-Infektionen bei normalen sowie immungeschwächten Patienten. Eine Wirksamkeit bei HSV- oder VZV-Enzephalotiden ist bis jetzt nicht bewiesen. Parenteral verabreichtes Aciclovir eignet sich gleichfalls zur Prophylaxe rezidivierender HSV-Infektionen beim immungeschwächten Patienten, wenngleich die Latenzphase der Viren, d.h. die Rezidivneigung, nicht beeinflußt wird. Resistenzen sind in Einzelfällen beschrieben, jedoch klinisch bis jetzt nicht bedeutsam. Insgesamt ist Aciclovir ein vielversprechendes Virustatikum in der Behandlung von Herpes simplex- und Varizella-Zoster-Infektionen insbesondere bei immungeschwächten Patienten.
Ergänzungen (1988)
Aciclovir wurde bei Burroughs-Wellcome in den USA von Gertrude Elion und George H. Hitchings entwickelt. Sie erhielten 1988 den Nobelpreis für Medizin und Physiologie in Anerkennung für ihre Entdeckungen zu wichtigen biochemischen Prinzipien der Arzneimitteltherapie.
Ergänzungen (2008)
Aciclovir ist ein weit verbreitetes, gut verträgliches Arzneimittel. Es steht heute auch zur oralen Therapie zur Verfügung, obwohl die Resorption aus dem Gastrointestinaltrakt gering und sehr variabel ist. Aufgrund der besseren Bioverfügbarkeit besitzen Valaciclovir und Famciclovir, etwa zur oralen Therapie des Zoster, gewisse Vorteile. Für alle drei Virustatika gelten jedoch die folgenden Einschränkungen:
- Bei immunkompetenten Patienten mit Zoster kann nur dann mit einer relativ geringen Verkürzung des Krankheitsverlaufs gerechnet werden, wenn die Behandlung innerhalb von 72 Stunden nach Beginn der Symptomatik initiiert wird.
- Auch unter günstigen Bedingungen ist bei der Behandlung des Zosters nicht immer mit einer Beeinflussung der postzosterischen Schmerzen zu rechnen.
Bei intravenöser Verabreichung ist Aciclovir besonders bei immunsupprimierten Patienten ein zuverlässig wirksames Virustatikum, das zum Beispiel bei folgenden Indikationen angewandt wird:
- Herpes-simplex-Enzephalitis (auch bei Verdacht auf diese Erkrankung)
- Infektionen mit empfindlichen Viren (Varizellen, Zoster, Herpes simplex) bei HIV-infizierten Personen
- Infektionen mit empfindlichen Viren bei immunsupprimierten Patienten (z.B. mit hämatologischen Grunderkrankungen oder nach Organtransplantation)
- Erstmalige, schwere Erkrankung an Herpes genitalis bei immunkompetenten Patienten
- Herpes-simplex-Infektion bei Neugeborenen.
Anwendung während der Schwangerschaft
Bei der intravenösen Therapie von Infektionen durch HSV oder VZV mit Aciclovir in der Schwangerschaft muß zwischen dem möglichen therapeutischen Nutzen und eventuellen Risiken für das Ungeborene abgewogen werden. Im Tierversuch erwies sich Aciclovir in relativ hohen Dosierungen als teratogen.
Auf die folgenden Übersichtsarbeiten soll hingewiesen werden:
Wagstaff AJ,
Faulds D, Goa KL. Aciclovir. A reappraisal of its antiviral activity, pharmacokinetic properties and therapeutic efficacy. Drugs 1994; 47: 153-205
Beutner KR,
Friedman DJ, Forszpaniak C, Andersen PL, Wood MJ. Valaciclovir compared with acyclovir for improved therapy for herpes zoster in immunocompetent adults. Antimicrob Agents Chemother.
1995;39:1546-53.
DWORKIN RH, JOHNSON RW et al. Recommendations for the management of herpes zoster. Clin Infect Dis. 2007 Jan 1;44 Suppl 1:S1-26.
ARORA A,
MENDOZA N et al. Double-blind study comparing 2 dosages of valacyclovir hydrochloride for the treatment of uncomplicated herpes zoster in immunocompromised patients 18 years of age and older.
J Infect Dis. 2008 May 1;197(9):1289-95.
BOMGAARS L,
THOMPSON P et al. Valacyclovir and acyclovir pharmacokinetics in immunocompromised children. Pediatr Blood Cancer. 2008 Oct;51(4):504-8.
KAMEI S,
SEKIZAWA T et al. Evaluation of combination therapy using aciclovir and corticosteroid in adult patients with herpes simplex virus encephalitis. J Neurol Neurosurg Psychiatry. 2005
Nov;76(11):1544-9.
TORRE D, TAMBINI R. Acyclovir for treatment of infectious mononucleosis: a meta-analysis.
Scand J Infect Dis. 1999;31(6):543-7.