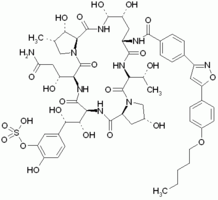
Micafungin
ein weiteres Arzneimittel zur Behandlung von Candida-Infektionen
Unveränderter Text aus Heft 2, 2009
Aktuelle Ergänzungen am Ende des Textes
Die Zahl der Patienten mit einem hohen Risiko für systemische Pilzinfektionen nimmt seit Jahren zu. Im Vordergrund stehen dabei Patienten mit Immunsuppression als Folge von Krebserkrankungen,
Organtransplantationen oder Autoimmunerkrankungen. Hinsichtlich der Häufigkeit steht Candida heute an Platz vier der aus dem Blut isolierten Erreger bei nosokomialen Infektionen. Vor diesem
Hintergrund ist die Entwicklung neuer Antimykotika zur Behandlung systemischer Pilzinfektionen zu begrüßen. Seit der Einführung von Caspofungin (CANCIDAS) im Jahre 2002 haben sich Echinocandine als besser verträgliche Alternative
zum Amphotericin B (AMPHOTERICIN B u.a.)
bewährt und werden zunehmend häufig angewandt. Diese Wirkstoffgruppe wurde durch Anidulafungin (ECALTA) einige Jahre später erweitert. Seit kurzem ist Micafungin (MYCAMINE) als ein drittes Echinocandin auf dem europäischen Markt. In den USA ist es bereits
seit 2005 verfügbar.1,2,3
Chemische Struktur, antimykotische Wirkung
Micafungin ist ein zyklisches Hexapeptid mit einer langen Seitenkette, die im Rahmen der halbsynthetischen Herstellung modifiziert wird. Die
Ausgangsverbindung wurde bereits 1989 entdeckt; sie unterscheidet sich von anderen Echinocandinen durch eine Sulfatgruppe, die dem Molekül eine ausreichende Wasserlöslichkeit verleiht. Im Präparat
MYCAMINE liegt der Wirkstoff als Natriumsalz vor.
Es wirkt entweder fungistatisch oder fungizid durch Hemmung des Enzyms 1,3-β-D-Glucansynthase.
1,3-β-D-Glucan ist ein wesentlicher Bestandteil der Pilzzellwand, der im Säugetierorganismus
nicht vorkommt. Die Hemmung des Enzyms führt zur Destabilisierung der Zellwandstruktur und schließlich zur Lyse der Pilzzelle.
Zum Wirkungsspektrum von Micafungin gehören Candida-Arten (C. albicans, C. glabrata, C. tropicalis, C. krusei u.a). Die minimalen Hemmkonzentrationen
dieser Erreger liegen ganz überwiegend deutlich unter 1 mg/l. Auch Isolate mit Resistenz gegen Fluconazol (DIFLUCAN u.a.) werden erfasst. Die Wachstumszonen der Hyphen von Aspergillus-Arten werden ebenfalls beeinflusst, gegen diese
Pilze wirkt Micafungin fungistatisch. Hinsichtlich der antimykotischen Aktivität unterscheidet sich Micafungin damit praktisch nicht von den anderen beiden Echinocandinen.
Pharmakokinetische Eigenschaften
Micafungin wird einmal täglich als einstündige Infusion verabreicht. Die empfohlene Dosierung beträgt bei einem Körpergewicht von mehr als 40 Kilogramm und
einmal täglicher Gabe 50 mg (Prophylaxe von Candida-Infektionen), 100 mg (invasive Candidiasis) beziehungsweise 150 mg (ösophageale Candidiasis). Eine Dosisanpassung bei Patienten mit eingeschränkter
Nierenfunktion ist nicht erforderlich. Der Wirkstoff liegt im Blut zu mehr als 99 Prozent an Plasmaproteine, hauptsächlich an Albumin, gebunden vor. Das Verteilungsvolumen wurde mit 18 bis 19 l
berechnet. Es wurden mehrere Metaboliten der Substanz nachgewiesen. Durch das Enzym Arylsulfatase entsteht der Metabolit M-1, der anschließend durch die Catechol-O-methyltransferase in die
Methoxyform (M-2) überführt wird. In vitro ist der Wirkstoff ein Substrat von CYP3A, die Hydroxylierung zählt jedoch nicht zu den Hauptstoffwechselwegen von Micafungin. Die mittlere terminale
Halbwertzeit liegt bei 10 bis 17 Stunden. Die Substanz wird ganz überwiegend extrarenal eliminiert.
Therapeutische Wirksamkeit
Die Wirksamkeit von Micafungin wurde in mehreren Studien im Vergleich mit anderen Antimykotika untersucht.4,5,6,7 Im direkten Vergleich konnten in einer
dreiarmigen Doppelblindstudie an insgesamt 595 Patienten mit systemischer Candida-Infektion keine Unterschiede in der Wirksamkeit zwischen Caspofungin und Micafungin festgestellt werden. Caspofungin
wurde in der üblichen Dosierung von 50 mg (initial 70 mg) verabreicht, Micafungin war in täglichen Dosierungen von 100 mg und 150 mg gleichwirksam wie Caspofungin. In einer weiteren Doppelblindstudie
war Micafungin bei insgesamt fast 400 Patienten mit Candidämie und invasiver Candidiasis ebenso wirksam wie liposomales Amphotericin B (AMBISOME). Der primäre Endpunkt (klinisches und mykologisches
Ansprechen am Ende der Therapie) wurde in beiden Gruppen in knapp 90 Prozent der Fälle erreicht. Im Vergleich von Micafungin (150 mg) und Fluconazol (200 mg) bei der Behandlung der ösophagealen
Candidiasis wurden in beiden Gruppen Ansprechraten von jeweils etwa 87 Prozent beobachtet. Bei der Prävention einer Mykose bei 882 erwachsenen und pädiatrischen Patienten, die eine
Knochenmarktransplantation erhielten, war Micafungin in einer Dosierung für Erwachsene von 50 mg täglich wirksamer als Fluconazol in einer Dosierung von 400 mg. Kinder erhielten Dosierungen von 1
mg/kg bzw. 8 mg/kg Körpergewicht. Unter Micafungin entwickelten 80 Prozent der Patienten keine Mykose gegenüber 73,5 Prozent der Patienten, die Fluconazol erhielten.
Interaktionen, Verträglichkeit, Toxizität
Die Behandlung mit Micafungin ist mit einem geringen Risiko für Cytochrom-P450-vermittelte Arzneimittelinteraktionen verbunden. Zum Beispiel sollen die
Patienten bei gleichzeitiger Behandlung mit Sirolimus (RAPAMUNE), Nifedipin (ADALAT u.a.) oder Itraconazol (SEMPERA u.a.) hinsichtlich toxischer Wirkungen dieser Arzneistoffe überwacht werden, weil die Exposition gegenüber diesen
Stoffen im Mittel um ca. 20% erhöht ist. Gegebenenfalls ist die Dosierung von Sirolimus, Nifedipin oder Itraconazol zu reduzieren.
Bei der Entscheidung zur Therapie mit dem neuen Echinocandin sollte laut Fachinformation MYCAMINE „in Betracht gezogen werden, dass ein Risiko zur Lebertumorbildung besteht“. Das Präparat ist daher
nur anzuwenden, wenn andere Antimykotika nicht geeignet sind. Die Relevanz des hepatokarzinogenen Potenzials für die therapeutische Anwendung beim Menschen ist nicht bekannt. Bedenklich erscheint,
dass die Exposition im Tierexperiment an dem vermutlichen Schwellenwert für Tumorentwicklung im selben Bereich lag, wie die klinische Exposition. Die Behandlungsdauer in der Toxizitätsstudie an
Ratten war zwar länger als die übliche Dauer einer antimykotischen Therapie, aber mit drei bzw. sechs Monaten kürzer, als in Standard-Kanzerogenitätsstudien. Die Tumore wurden mehrere Monate nach
Ende der Behandlung beobachtet.
Die Gesamthäufigkeit unerwünschter Wirkungen auf die Leber bei mit Micafungin behandelten Patienten in klinischen Prüfungen betrug 8,6 Prozent (260/3028). Nur bei wenigen Patienten musste die
Behandlung aufgrund einer hepatischen Symptomatik abgebrochen werden. Während der Behandlung mit Micafungin muss die Leberfunktion sorgfältig überwacht werden. Bei einem Anstieg der Leberenzyme muss
die Therapie beendet werden. Vor allem bei Patienten mit bereits bestehenden Lebererkrankungen darf das Antimykotikum nur nach sorgfältiger Nutzen-Risiko-Abwägung eingesetzt werden.
Die häufigsten während der klinischen Prüfung beobachteten Nebenwirkungen des neuen Arzneimittels sind Störungen des Gastrointestinaltraktes (Übelkeit, Erbrechen, Durchfall, Bauchschmerzen),
Elektrolytstörungen (Hypokaliämie, Hypomagnesämie), sowie Kopfschmerzen, Venenentzündungen an der Infusionsstelle, Ausschlag und Fieber. Auch Blutbildveränderungen (Leukopenie, Anämie) können
auftreten. In Einzelfällen wurden Patienten beschrieben, die während der Behandlung mit Micafungin aufgrund massiver Hämolyse ein Nierenversagen entwickelten.
ZUSAMMENFASSUNG
Micafungin (MYCAMINE) ist ein weiteres Antimykotikum aus der Gruppe der Echinocandine zur Behandlung systemischer
Pilzinfektionen. Es hemmt das Enzym 1,3-β-D-Glucansynthase und stört dadurch einen regelrechten
Aufbau der Zellwand der Erreger. Gegenüber Candida-Arten wirkt es fungizid oder fungistatisch. Nach intravenöser Verabreichung wird es in der Leber metabolisiert; die Abbauprodukte werden überwiegend
mit dem Stuhl eliminiert. Die Eliminationshalbwertzeit liegt bei 10 bis 17 Stunden. In mehreren Doppelblindstudien wurde die therapeutische Wirksamkeit bei systemischen Candida-Infektionen gezeigt;
bei Aspergillus-Infektionen ist das Präparat nicht geprüft und nicht zugelassen. Die wichtigsten unerwünschten Wirkungen betreffen den Gastrointestinaltrakt. Die Leberfunktion muss kontrolliert
werden. Daneben wurden Blutbildveränderungen und Hautreaktionen beobachtet. Bei der Nutzen-Risiko-Abwägung einer Therapie mit dem Antimykotikum muss das tierexperimentell festgestellte,
hepatokanzerogene Potenzial der Substanz berücksichtigt werden.
1. HASHIMOTO
S. Micafungin: a sulfated echinocandin.
J Antibiot (Tokyo). 2009
Jan;62(1):27-35.
2. Fachinfo MYCAMINE Astellas Pharma, Leiderdorp (Niederlande)
3. CROSS SA, SCOTT LJ. Micafungin: a review of its use in
adults for the treatment of invasive and
oesophageal candidiasis, and as
prophylaxis against Candida infections.
Drugs. 2008;68(15):2225-55.
4. KUSE ER, CHETCHOTISAKD P et al. Micafungin Invasive
Candidiasis Working Group. Micafungin
versus liposomal amphotericin B for
candidaemia and invasive candidosis: a phase III randomised
double-blind trial. Lancet. 2007 May
5;369(9572):1519-27.
5. DE WET NT, BESTER AJ et al. A randomized, double
blind, comparative trial of micafungin (FK463) vs.
fluconazole for the treatment of
oesophageal candidiasis.
Aliment Pharmacol Ther. 2005 Apr
1;21(7):899-907.
6. VAN BURIK JA, RATANATHARATHORN V et al. Micafungin
versus fluconazole for prophylaxis against
invasive fungal infections during
neutropenia in patients undergoing hematopoietic stem cell
transplantation. Clin Infect
Dis. 2004 Nov 15;39(10):1407-16.
7. NANRI T, IWANAGA E et al. Micafungin-induced immune hemolysis
attacks.
Int J Hematol. 2009
Aktuelle Ergänzungen (Dezember 2009)
Seit der Erstellung und Veröffentlichung dieses Artikels in der Zeitschrift für Chemotherapie (Heft 2, 2009) sind zahlreiche
weitere Arbeiten über Micafungin publiziert worden. Insbesondere soll an dieser Stelle auf die folgende Arbeit hingewiesen werden:
HORN DL,
NEOFYTOS D et al. Epidemiology and outcomes of candidemia in 2019 patients: data from the prospective antifungal therapy
alliance registry. Clin Infect Dis. 2009 Jun 15;48(12):1695-703.